工业上常用焦炭和二氧化硅在电炉中发生氧化还原反应制取粗硅,反应方程式为:2C+SiO2
Si+2CO↑.下列叙述不正确的是( )
| ||
| A、C是还原剂,发生还原反应 |
| B、SiO2是氧化剂,在反应中被还原 |
| C、氧化还原反应的实质是电子的转移 |
| D、氧化还原反应中电子转移的总数与化合价升降总数相等 |
“酸化”是实验中经常采用的方法,下列酸化过程正确的是( )
| A、抑制Fe2+的水解,用稀硝酸酸化 |
| B、提高高锰酸钾的氧化能力,用盐酸酸化 |
| C、检验SO42-时,用盐酸酸化 |
| D、检验Cl-时,用稀硫酸酸化 |
生产生活中的许多现象与化学反应有关,下列现象与氧化还原反应无关的是( )
| A、铜铸塑像上出现铜绿[Cu2(OH)2CO3] |
| B、工业制备氯气 |
| C、金属冶炼 |
| D、服用含Al(OH)3的胃药可以治疗胃酸过多 |
有关如图所示装置的叙述不正确的是( )
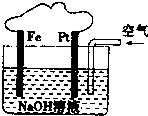

| A、该装置内可发生原电池反应 |
| B、该装置中Pt为正极,电极反应为:O2+2H2O+4e-=4OH- |
| C、溶液中会出现红褐色的沉淀 |
| D、该装置中Fe为阴极,电极反应为:Fe-2e-+2OH-=Fe(OH)2 |
下列说法或表示方法中正确的是( )
| A、化学变化的实质是旧键的断裂和新键的生成,有物质变化但不一定有能量变化 |
| B、氢气的燃烧热为285.8kJ?mol-1,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=285.8kJ?mol-1 |
| C、Ba(OH)2?8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l)△H<0 |
| D、已知中和热为57.3kJ?mol-1,若将含0.5molH2SO4的浓溶液与含1molNaOH的溶液混合,放出的热量要大于57.3kJ |
下列有关化学反应能量变化的叙述一定正确的是( )
| A、生成物总能量大于反应物总能量,该反应为放热反应 |
| B、一个化学反应需要加热才能进行,该反应为吸热反应 |
| C、应用盖斯定律,可计算某些难以直接测量的化学反应焓变 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H不同 |
 原子序数小于36的X、Y、Z、W四种元素,其中X是原子半径最小的元素,Y原子基态时s能级上的电子总数是p能级上电子总数的2倍.Z原子基态时2p原子轨道上有3个未成对的电子,W的外围电子构型是3d104s1.回答下列问题:
原子序数小于36的X、Y、Z、W四种元素,其中X是原子半径最小的元素,Y原子基态时s能级上的电子总数是p能级上电子总数的2倍.Z原子基态时2p原子轨道上有3个未成对的电子,W的外围电子构型是3d104s1.回答下列问题: (1)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.
(1)A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸.