题目内容
在Fe3O4+4CO
3Fe+4CO2的中, 是氧化剂, 是还原剂, 元素被还原.
| ||
考点:氧化还原反应
专题:氧化还原反应专题
分析:Fe3O4+4CO
3Fe+4CO2中,Fe元素的化合价降低,C元素的化合价升高,以此来解答.
| ||
解答:
解:Fe3O4+4CO
3Fe+4CO2中,Fe元素的化合价降低,则Fe3O4为氧化剂;C元素的化合价升高,CO为还原剂,在反应中Fe元素被还原,
故答案为:Fe3O4;CO;Fe.
| ||
故答案为:Fe3O4;CO;Fe.
点评:本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,题目难度不大.

练习册系列答案
相关题目
今年世界地球日主题为“珍惜地球资源 转变发展方式”.下列做法违背该主题的是( )
| A、利用秸杆、垃圾发电 |
| B、利用太阳能、地热能等清洁能源 |
| C、回收利用废旧金属 |
| D、大量开采、使用化石燃料 |
有关如图所示装置的叙述不正确的是( )
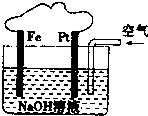

| A、该装置内可发生原电池反应 |
| B、该装置中Pt为正极,电极反应为:O2+2H2O+4e-=4OH- |
| C、溶液中会出现红褐色的沉淀 |
| D、该装置中Fe为阴极,电极反应为:Fe-2e-+2OH-=Fe(OH)2 |
铅的冶炼大致过程如下:下列说法正确的是( )
①富集:将方铅矿(PbS)进行浮选;
②焙烧:2PbS+3O2
2PbO+2SO2;
③制粗铅:PbO+C
Pb+CO;PbO+CO
Pb+CO2.
①富集:将方铅矿(PbS)进行浮选;
②焙烧:2PbS+3O2
| ||
③制粗铅:PbO+C
| ||
| ||
| A、浮选法富集方铅矿的过程属于化学变化 |
| B、方铅矿焙烧反应中,PbS是还原剂,发生还原反应 |
| C、过程②中,制取1molPbO共转移2mol电子 |
| D、将1molPbS冶炼成Pb理论上至少需要6g碳 |
已知燃烧1mol葡萄糖(Mr=180)的放出的热量是2804kJ?mol-1,当氧化1g葡萄糖时放出的热量是( )
| A、51.9kJ |
| B、15.6kJ |
| C、155.8kJ |
| D、26.0kJ |
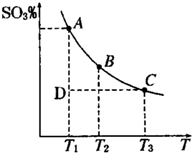 运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义.