0 129353 129361 129367 129371 129377 129379 129383 129389 129391 129397 129403 129407 129409 129413 129419 129421 129427 129431 129433 129437 129439 129443 129445 129447 129448 129449 129451 129452 129453 129455 129457 129461 129463 129467 129469 129473 129479 129481 129487 129491 129493 129497 129503 129509 129511 129517 129521 129523 129529 129533 129539 129547 203614

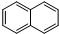 )的衍生物;
)的衍生物;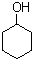 为原料制备化合物B的合成路线流程图(无机试剂任选).合成路线流程图示例如下:H2C═CH2
为原料制备化合物B的合成路线流程图(无机试剂任选).合成路线流程图示例如下:H2C═CH2
 ),请在方框内写出合成路线流程(无机试剂任选).注:合成路线流程的书写格式参照如下示例:
),请在方框内写出合成路线流程(无机试剂任选).注:合成路线流程的书写格式参照如下示例:
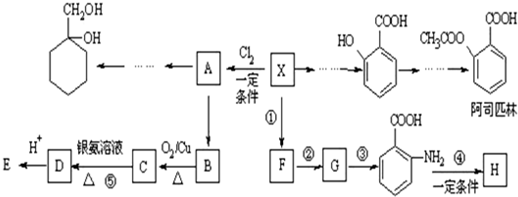
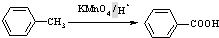
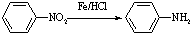 (苯胺,易被氧化)
(苯胺,易被氧化)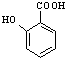 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有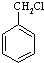 和其他无机物合成
和其他无机物合成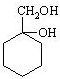 最合理的方案(不超过4步),请在答题纸的方框中表示.例:
最合理的方案(不超过4步),请在答题纸的方框中表示.例: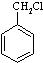
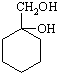
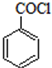 )是合成药品的重要中间体.请写出以苯、乙醚、甲醛为原料制备苯甲酰氯的合成路线流程图(无机试剂任用).合成路线流程图示例如下:
)是合成药品的重要中间体.请写出以苯、乙醚、甲醛为原料制备苯甲酰氯的合成路线流程图(无机试剂任用).合成路线流程图示例如下: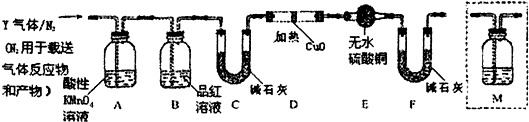
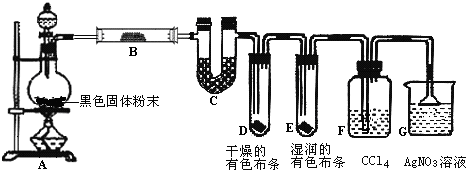
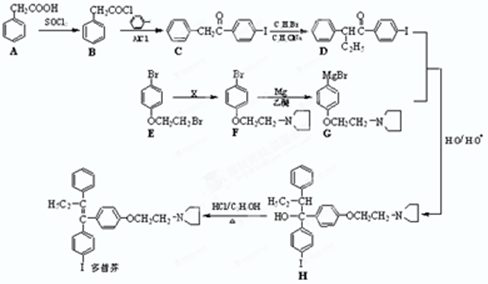
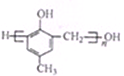 )的合成路线如下:
)的合成路线如下: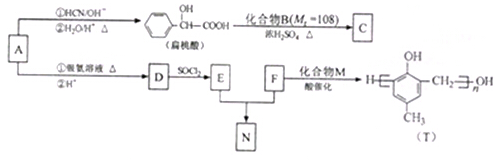
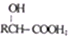

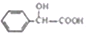 )有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体共有
)有多种同分异构体,属于甲酸酯且含酚羟基的同分异构体共有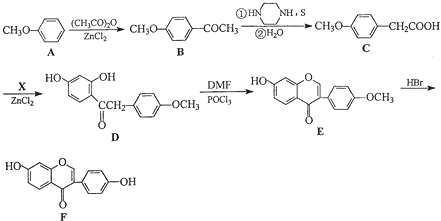
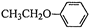 和(CH3CO)2O为原料制备药物中间体
和(CH3CO)2O为原料制备药物中间体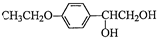 的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2
的合成路线流程图(无机试剂任用).合成路线流程图示例如下:H2C=CH2