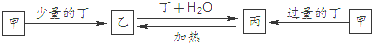在标准状况下,将aLNH3完全溶于水得到VmL氨水,所得溶质的物质的量浓度为c mol/L.下列叙述中不正确的是( )
A、C=
| ||
B、已知常温下,氨水的电离常数为Ka,则pH约等于14+lg
| ||
| C、上述溶液中再加入0.5VmL同浓度稀盐酸,充分反应后c(Cl-)=c(NH4+)+c(NH3?H2O) | ||
| D、上述溶液中再加入VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
反应2H2S(g)?2H2(g)+S2(g)△H>0,其他条件不变,下列说法正确的是( )
| A、加入催化剂,反应路径将发生改变,△H也将随之改变 |
| B、升高温度,正逆反应速率都增大,H2S分解率也增大 |
| C、增大压强,平衡向逆反应方向移动,体系温度降低 |
| D、恒容体系,充入H2重新达到平衡后,H2浓度将减小 |
在一定条件下,对于反应2A(g)+B(g)?2C(g),下列说法中正确的是( )
A、此反应的平衡常数K=
| ||
| B、改变条件该反应的平衡常数K一定不变 | ||
| C、改变压强并加入催化剂,平衡常数会随之变化 | ||
| D、平衡时增大A和B的浓度,平衡常数会减小 |
甲、乙、丙、丁四种物质分别含2种或3种元素,它们的分子中各含18个电子.甲是气态氢化物,在水中分步电离出两种阴离子.下列推断不合理的是( )
| A、某钠盐溶液含甲电离出的阴离子,则该溶液显碱性且能与酸反应 |
| B、乙与氧气的摩尔质量相同,则乙可能是N2H4或CH3OH |
| C、丙中含有第2周期ⅣA族的元素,则丙一定是甲烷的同系物 |
| D、丁和甲中各元素质量比相同,则丁中一定含有-1价的元素 |
已知有以下的物质相互转化关系,A是常见的金属单质,能被磁铁吸引.
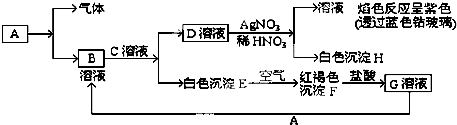
(1)试回答:写出B的化学式 C的化学式 H的化学式
(2)写出由E转变成F的化学方程式 .
(3)向G溶液加入A的有关离子反应方程式 .

(1)试回答:写出B的化学式
(2)写出由E转变成F的化学方程式
(3)向G溶液加入A的有关离子反应方程式