题目内容
已知甲、乙、丙三种化合物中都含有同种金属元素,它们的焰色反应为黄色,丁通常情况下是一种无色无味气体,能使澄清石灰水变浑浊.4种物质之间有如图所示的转化关系(转化过程申部分产物未标出).
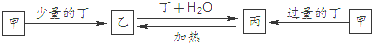
(1)写出甲的化学式: .
(2)写出乙→丙的化学方程式: .
(3)向乙溶液中逐滴加入盐酸,现象为: .
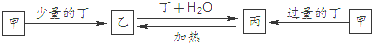
(1)写出甲的化学式:
(2)写出乙→丙的化学方程式:
(3)向乙溶液中逐滴加入盐酸,现象为:
考点:无机物的推断,钠的重要化合物
专题:元素及其化合物
分析:甲、乙、丙三种化合物中都含有同种金属元素,它们的焰色反应为黄色说明都含有Na元素,丁通常情况下是一种无色无味气体,能使澄清石灰水变浑浊,则丁是CO2,乙和二氧化碳、水反应生成丙,丙加热生成丁,则乙是Na2CO3、丙是NaHCO3,甲和少量二氧化碳反应生成碳酸钠、和过量二氧化碳反应生成碳酸氢钠,则甲是NaOH,再结合题目解答.
解答:
解:甲、乙、丙三种化合物中都含有同种金属元素,它们的焰色反应为黄色说明都含有Na元素,丁通常情况下是一种无色无味气体,能使澄清石灰水变浑浊,则丁是CO2,乙和二氧化碳、水反应生成丙,丙加热生成丁,则乙是Na2CO3、丙是NaHCO3,甲和少量二氧化碳反应生成碳酸钠、和过量二氧化碳反应生成碳酸氢钠,则甲是NaOH,
(1)通过以上分析知,甲的化学式:NaOH,故答案为:NaOH;
(2)乙是碳酸钠、丙是碳酸氢钠,乙和二氧化碳、水反应生成丙,乙→丙的化学方程式:Na2CO3+CO2+H2O=2 NaHCO3,故答案为:Na2CO3+CO2+H2O=2 NaHCO3;
(3)乙是碳酸钠,向碳酸钠中滴加稀盐酸,稀盐酸先和碳酸钠反应生成碳酸氢钠和NaOH,当完全转化为碳酸氢钠后,继续滴加稀盐酸,稀盐酸和碳酸氢钠反应生成二氧化碳、水和NaOH,所以看到的现象是开始无气泡,后来产生气泡,故答案为:开始无气泡,后来产生气泡.
(1)通过以上分析知,甲的化学式:NaOH,故答案为:NaOH;
(2)乙是碳酸钠、丙是碳酸氢钠,乙和二氧化碳、水反应生成丙,乙→丙的化学方程式:Na2CO3+CO2+H2O=2 NaHCO3,故答案为:Na2CO3+CO2+H2O=2 NaHCO3;
(3)乙是碳酸钠,向碳酸钠中滴加稀盐酸,稀盐酸先和碳酸钠反应生成碳酸氢钠和NaOH,当完全转化为碳酸氢钠后,继续滴加稀盐酸,稀盐酸和碳酸氢钠反应生成二氧化碳、水和NaOH,所以看到的现象是开始无气泡,后来产生气泡,故答案为:开始无气泡,后来产生气泡.
点评:本题考查无机物推断,侧重考查分析、推断能力,涉及碳酸钠、碳酸氢钠、NaOH之间的转化及焰色反应,以焰色反应、反应物的量及反应条件进行推断即可,题目难度不大.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案 优加精卷系列答案
优加精卷系列答案
相关题目
在一定条件下,对于反应2A(g)+B(g)?2C(g),下列说法中正确的是( )
A、此反应的平衡常数K=
| ||
| B、改变条件该反应的平衡常数K一定不变 | ||
| C、改变压强并加入催化剂,平衡常数会随之变化 | ||
| D、平衡时增大A和B的浓度,平衡常数会减小 |
将浓度都为1mol/L的Na2CO3溶液和稀H2SO4按体积比2:1混合,则下列说法正确的是( )
| A、混合溶液的pH<7 |
| B、混合溶液中:c(SO42-)+c(OH-)<c(HCO3-)+c(H2CO3)+c(CO32-) |
| C、混合溶液中:c(Na+)+c(H+)<2[c(SO42-)+c(CO32-)] |
| D、混合溶液中离子浓度大小顺序是:c(Na+)>c(HCO3-)>c(OH-)>c(SO42-)>c(H+) |
下列有关说法正确的是( )
| A、明矾水解时产生具有吸附性的胶体粒子,可作漂白剂 |
| B、酸雨是PH小于7的雨水 |
| C、自行车钢架生锈主要是化学腐蚀所致 |
| D、大气中CO2含量的增加会导致温室效应加剧 |
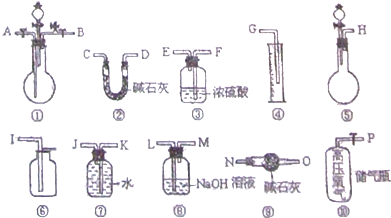
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.