题目内容
在标准状况下,将aLNH3完全溶于水得到VmL氨水,所得溶质的物质的量浓度为c mol/L.下列叙述中不正确的是( )
A、C=
| ||
B、已知常温下,氨水的电离常数为Ka,则pH约等于14+lg
| ||
| C、上述溶液中再加入0.5VmL同浓度稀盐酸,充分反应后c(Cl-)=c(NH4+)+c(NH3?H2O) | ||
| D、上述溶液中再加入VmL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
考点:离子浓度大小的比较,pH的简单计算
专题:
分析:A、根据c=
来计算;
B、根据溶液中C(OH-)=C?Ka来计算;
C、根据物料守恒来分析;
D、加入VmL同浓度稀盐酸,两者完全反应得NH4Cl溶液;
| n |
| V |
B、根据溶液中C(OH-)=C?Ka来计算;
C、根据物料守恒来分析;
D、加入VmL同浓度稀盐酸,两者完全反应得NH4Cl溶液;
解答:
解:A、c=
=
=
mol/L,故A正确;
B、溶液中C(OH-)=C?Ka,C(H+)=
=
,故pH=-lgC(OH-)=14+lg
,故B正确;
C.所得VmL氨水与等浓度0.5VmL的盐酸反应,生成的氯化铵与所剩氨水的物质的量之比为1:1,所有根据物料守恒,应有2c(Cl-)=c(NH4+)+c(NH3?H2O),故C错误;
D、加入VmL同浓度稀盐酸,两者完全反应得NH4Cl溶液,溶液显酸性,故有c(H+)>c(OH-),根据电荷守恒可知,c(Cl-)>c(NH4+),而盐类的单水解程度很小,故有:c(Cl-)>c(NH4+)>c(H+)>c(OH-),故D正确;
故选C.
| n |
| V |
| ||
| V×10-3L |
| 1000a |
| 22.4V |
B、溶液中C(OH-)=C?Ka,C(H+)=
| Kw |
| C(OH-) |
| 10-14 |
| C?Kw |
| cKa |
C.所得VmL氨水与等浓度0.5VmL的盐酸反应,生成的氯化铵与所剩氨水的物质的量之比为1:1,所有根据物料守恒,应有2c(Cl-)=c(NH4+)+c(NH3?H2O),故C错误;
D、加入VmL同浓度稀盐酸,两者完全反应得NH4Cl溶液,溶液显酸性,故有c(H+)>c(OH-),根据电荷守恒可知,c(Cl-)>c(NH4+),而盐类的单水解程度很小,故有:c(Cl-)>c(NH4+)>c(H+)>c(OH-),故D正确;
故选C.
点评:本题考查了物质的量浓度和pH的计算和盐溶液中离子浓度的大小笔记以及物料守恒,难度不大.

练习册系列答案
相关题目
甲、乙、丙、丁四种物质分别含2种或3种元素,它们的分子中各含18个电子.甲是气态氢化物,在水中分步电离出两种阴离子.下列推断不合理的是( )
| A、某钠盐溶液含甲电离出的阴离子,则该溶液显碱性且能与酸反应 |
| B、乙与氧气的摩尔质量相同,则乙可能是N2H4或CH3OH |
| C、丙中含有第2周期ⅣA族的元素,则丙一定是甲烷的同系物 |
| D、丁和甲中各元素质量比相同,则丁中一定含有-1价的元素 |
将浓度都为1mol/L的Na2CO3溶液和稀H2SO4按体积比2:1混合,则下列说法正确的是( )
| A、混合溶液的pH<7 |
| B、混合溶液中:c(SO42-)+c(OH-)<c(HCO3-)+c(H2CO3)+c(CO32-) |
| C、混合溶液中:c(Na+)+c(H+)<2[c(SO42-)+c(CO32-)] |
| D、混合溶液中离子浓度大小顺序是:c(Na+)>c(HCO3-)>c(OH-)>c(SO42-)>c(H+) |
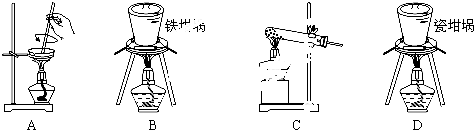
下列实验装置、试剂选用或操作正确的是( )
A、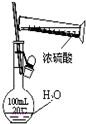 稀释浓硫酸 |
B、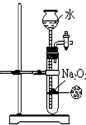 制备少量O2 |
C、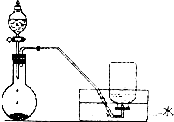 浓氨水和生石灰反应制取氨气 |
D、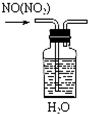 除去NO中的NO2 |
下列有关金属腐蚀与防护的说法正确的是( )
| A、在铁门上焊接铜块能防腐蚀 |
| B、镀锡铁制品的镀层破损后,镀层仍能对铁制品起保护作用 |
| C、钢柱在水下部分比在空气与水交界处更容易腐蚀 |
| D、在海轮外壳连接锌块,保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
为证明亚硫酸钠被部分氧化变质成硫酸钠,下列可以选择的合理实验方案有 ( )
| A、与消石灰共热,并将湿润红色石蕊试纸置于试管口 |
| B、先加入足量的稀硫酸,再滴入适量BaCl2溶液 |
| C、先加入足量的稀盐酸,再滴入适量BaCl2溶液 |
| D、加入足稀硫酸溶液直至过量,充分反应后过滤 |