下列说法正确的是( )
| A、4.6g有机物C2H6O的分子结构中含有的C-H键数目一定为0.5NA | ||||||||||
| B、一定温度下,氯化铵水解离子方程式:NH+4+H2O?NH3?H2O+H+,若用KW表示的离子积,Kb表示氨水电离常数,则氯化铵水解平衡常数K=KW/Kb | ||||||||||
| C、已知反应:2Fe3++2I-=2Fe2++I2:2Co(OH)3+2Cl-+6H+=2Co2++Cl2↑+6H2O:2Fe(OH)2+I2+2OH-=2Fe(OH)3+2I-;则在酸性溶液中氧化性:Fe3+>Co(OH)3>I2 | ||||||||||
D、已知
|
某原电池装置如图所示.电池总反应为:2Ag+Cl2═2AgCl.下列说法正确的是( )

| A、正极反应为Cl2-2e-=2Cl- |
| B、放电时H+从右侧经阳离子交换膜移向左侧 |
| C、电路中转移0.01 mole-时,交换膜左侧溶液中减少0.01 mol离子 |
| D、若用NaCl溶液代替盐酸,电池的总反应不会改变 |
分子式是 C8H10 的芳香烃在FeBr3做催化剂的条件下和液溴发生反应,生成的一溴代物有( )种.
| A、5 | B、8 | C、9 | D、10 |
下列说法正确的是( )
A、相同条件下,结合质子的能力:OH->AlO2->CO32->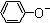 >HCO3->CH3COO- >HCO3->CH3COO- |
B、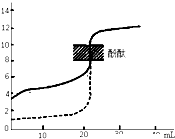 如图表示用0.1mol/LNaOH溶液分别滴定相同物质的量浓度和相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线 |
| C、一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率,平衡常数保持不变 |
| D、恒容密闭容器中进行的反应A(g)?B(g)+C(g),在其它条件不变情况下,再充入一定量的A气体,A的转化率将增大 |
 常温下,用 0.1000mol?L-1NaOH溶液滴定 20.00mL 0.1000mol?L-1CH3COOH溶液所得滴定曲线如图.下列说法不正确的是( )
常温下,用 0.1000mol?L-1NaOH溶液滴定 20.00mL 0.1000mol?L-1CH3COOH溶液所得滴定曲线如图.下列说法不正确的是( )| A、点①所示溶液中:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| B、点②所示溶液中:c(Na+)=c(CH3COO-) |
| C、点③所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) |
| D、滴定过程中可能出现:c(CH3COOH)>c(H+)>c(CH3COO-)>c(Na+)>c(OH-) |
反应Fe(s)+CO2(g)?FeO(s)+CO(g),700℃时平衡常数为1.47,900℃时平衡常数为2.15.下列说法正确的是( )
| A、升高温度该反应的正反应速率增大,逆反应速率减小 | ||
B、该反应的化学平衡常数表达式为K=
| ||
| C、绝热容器中进行该反应,温度不再变化,则达到化学平衡状态 | ||
| D、该反应的正反应是放热反应 |


