题目内容
12.下列各组离子中,因为发生氧化还原反应而不能共存的是( )| A. | K+、MnO4-、Na+、I- | B. | Mg2+、Na+、NO3-、CO32- | ||
| C. | AlO2-、NO3-、H+、SO42- | D. | CH3COO-、Na+、SO42-、H+、 |
分析 具有还原性的离子与具有氧化性的离子,发生氧化还原反应,不能共存,以此来解答.
解答 解:A.MnO4-、I-发生氧化还原反应,不能共存,故A选;
B.Mg2+、CO32-结合生成沉淀,因复分解反应不能共存,故B不选;
C.AlO2-、H+结合生成沉淀,因复分解反应不能共存,故C不选;
D.CH3COO-、H+结合生成弱酸,因复分解反应不能共存,故D不选;
故选A.
点评 本题考查离子共存,为高频考点,把握离子之间的反应为解答本题的关键,侧重分析与应用能力的考查,注意复分解反应、氧化还原反应的判断,题目难度不大.

练习册系列答案
相关题目
2.下列各组物质在溶液中反应时,以任意量混合均能用同一离子方程式表示的是( )
| A. | Ca(HCO3)2溶液和Ca(OH)2溶液 | B. | NaHCO3溶液和Ca(OH)2溶液 | ||
| C. | Na2CO3溶液和稀盐酸 | D. | Na和稀盐酸 |
20.用如图所示的装置电解KBr溶液制取KBrO3,生成16.7g KBrO3时理论上转移电子的物质的量为( )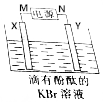

| A. | 0.1mol | B. | 0.2mol | C. | 0.4mol | D. | 0.6mol |
17.120℃时,将H2、C2H5OH、O2的混合气体通入盛有足量Na2O2的密闭容器中,用电火花不断点燃,反应完全后,体系内压强为零,则混合气体中,H2、C2H5OH、O2的物质的量之比可能是( )
| A. | 3:4:1 | B. | 3:1:2 | C. | 7:2:1 | D. | 9:3:1 |
4.用NaCl固体配制100mL2.00mol•L-1NaCl溶液,不需要用到的仪器是( )
| A. | 100mL容量瓶 | B. | 量筒 | C. | 玻璃棒 | D. | 烧杯 |
4.在新制饱和氯水中,若只改变某一条件,下列叙述正确的是( )
| A. | 再通入少量氯气,$\frac{c({H}^{+})}{c(Cl{O}^{-})}$减小 | |
| B. | 通入少量SO2,溶液漂白性增强 | |
| C. | 加入少量的碳酸钠粉末,pH增大,溶液漂白性增强 | |
| D. | 光照过程中,有气泡冒出,溶液的导电性减弱 |
5.研究电化学的装置如图所示,虚线框中可接a (电流计)或b (直流电源).下列说法错误的是( )

| A. | 接a,该装置将化学能转化为电能 | B. | 接a,石墨是正极 | ||
| C. | 接b,铁片连正极时被保护 | D. | 接b,石墨连正极时石墨上产生气泡 |