题目内容
1.A、B、C、D、E为原子序数依次增大的短周期主族元素.A的某种核素不含中子; B 是形成化合物种类最多的元素;C是地壳中含量最多的元素,E与C为同主族元素; C 与 D 可形成D2C和D2C2两种常见的离子化合物.下列说法正确的是( )| A. | 元素的非金属性C>A>B | |
| B. | C与A也可形成两种离子化合物 | |
| C. | 元素C、D、E形成的化合物溶于水后溶液呈中性 | |
| D. | 由C、E形成的化合物标准状况下不一定为气态 |
分析 A的某种核素不含中子,应为H元素; B 是形成化合物种类最多的元素,为C元素;C是地壳中含量最多的元素,为O元素,E与C为同主族元素,应为S元素; C 与 D 可形成D2C和D2C2两种常见的离子化合物,则D为Na元素,对应的氧化物为氧化钠、过氧化钠,结合对应单质、化合物的性质以及元素周期律解答该题.
解答 解:由以上分析可知A为H元素,B为C元素,C为O元素,D为Na元素,E为S元素,
A.H与C相比较,C易得到电子,非金属性较强,故A错误;
B.H与O形成的化合物为共价化合物,故B错误;
C.如生成Na2SO3,则对应的溶液呈碱性,故C错误;
D.如为SO3,则标准状况下为固体,故D正确.
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子结构、元素的性质推断元素为解答本题的关键,侧重分析与应用的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案
相关题目
11.有十种物质:①甲烷; ②聚乙烯;③苯;④苯乙烯;⑤邻二甲苯;⑥环己烷;⑦环己烯;⑧聚乙炔;⑨乙醇;⑩2-丁炔.既能使酸性高锰酸钾溶液褪色,又能使溴水因化学反应褪色的共有几种( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
12. 利用铅蓄电池对如图装置进行供电,能模拟植物光合作用,将简单无机物转化为O2和C3H8O,下列说法不正确的是( )
利用铅蓄电池对如图装置进行供电,能模拟植物光合作用,将简单无机物转化为O2和C3H8O,下列说法不正确的是( )
 利用铅蓄电池对如图装置进行供电,能模拟植物光合作用,将简单无机物转化为O2和C3H8O,下列说法不正确的是( )
利用铅蓄电池对如图装置进行供电,能模拟植物光合作用,将简单无机物转化为O2和C3H8O,下列说法不正确的是( )| A. | 该装置实现了将太阳能、电能转化为化学能 | |
| B. | b极上每生成0.1molO2,铅蓄电池的负极增重19.2g | |
| C. | a极上每生成0.1molC3H8O,有1.8mol电子发生转移 | |
| D. | 质子交换膜的作用是传导电子、平衡电荷,沟通回路 |
9.下列说法不正确的是( )
| A. | 油脂发生皂化反应能生成甘油 | |
| B. | 丙烷和2-甲基丙烷的一氯代物均为两种 | |
| C. | 酿酒过程中,葡萄糖可通过水解反应生成酒精 | |
| D. |  ≡C-COOH是高分子化合物 ≡C-COOH是高分子化合物 的单体 的单体 |
16.用下列实验装置进行相应的实验,能达到实验目的是( )
| A. | 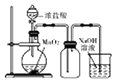 实验室制取Cl2 | B. | 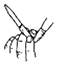 检查碱式滴定管是否漏液 | ||
| C. | 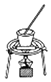 从食盐水中提取NaCl | D. | 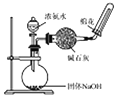 制备收集干燥的NH3 |
13.下列叙述正确的是( )
| A. | 以可逆反应为原理的原电池发生反应达平衡时,该电池仍有电流产生 | |
| B. | 使用催化剂能够降低正、逆反应的活化能和△H | |
| C. | 金属发生吸氧腐蚀时,被腐蚀的速率和溶解氧的浓度无关 | |
| D. | 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中氯离子和溴离子浓度的比值不变 |
1.NA代表阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,22.4LCl2与足量的铁粉反应,转移的电子数为3NA | |
| B. | 含23g钠元素的Na2O和Na2O2混合物中阴离子数目介于0.5NA和NA之间 | |
| C. | 在0℃、101kPa条件下,11.2L丁烷中含极性共价键数目为5NA | |
| D. | 5NH4NO3$\frac{\underline{\;△\;}}{\;}$4N2↑+2HNO3+9H2O中氧化产物比还原产物每多14g,转移电子数为15NA |
2. 一定温度下在密闭容器内进行着某一反应,X气体,Y气体的物质的量 随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在密闭容器内进行着某一反应,X气体,Y气体的物质的量 随反应时间变化的曲线如图.下列叙述中正确的是( )
 一定温度下在密闭容器内进行着某一反应,X气体,Y气体的物质的量 随反应时间变化的曲线如图.下列叙述中正确的是( )
一定温度下在密闭容器内进行着某一反应,X气体,Y气体的物质的量 随反应时间变化的曲线如图.下列叙述中正确的是( )| A. | 反应的化学方程式为2Y?X | B. | t1时,Y的浓度是X浓度的1.5倍 | ||
| C. | t2时,正、逆反应速率相等 | D. | t3时,逆反应速率大于正反应速率 |
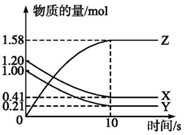 一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示: