题目内容
2.合成导电高分子化合物PPV的反应为: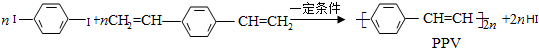
下列说法正确的是( )
| A. | PPV是聚苯乙炔 | |
| B. | 该反应为缩聚反应 | |
| C. | PPV与聚苯乙烯的最小结构单元组成相同 | |
| D. | 1 mol 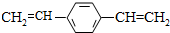 最多可与2 mol H2发生反应 最多可与2 mol H2发生反应 |
分析 由反应方程式可知PPV由对二碘苯与 发生缩聚反应生成,与苯乙炔、苯乙烯的加聚产物不同,以此解答该题.
发生缩聚反应生成,与苯乙炔、苯乙烯的加聚产物不同,以此解答该题.
解答 解:A.根据物质的分子结构可知该物质不是聚苯乙炔,故A错误;
B.该反应除产生高分子化合物外,还有小分子生成,属于缩聚反应,故B正确;
C.PPV与聚苯乙烯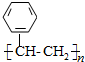 的重复单元不相同,故C错误;
的重复单元不相同,故C错误;
D.该物质一个分子中含有2个碳碳双键和苯环都可以与氢气发生加成反应,属于1mol  最多可以与5mol氢气发生加成反应,故D错误.
最多可以与5mol氢气发生加成反应,故D错误.
故选B.
点评 本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构尤其时高聚物的结构,难度不大.

练习册系列答案
相关题目
13.一定温度下,在3个体积均为1.0L的容量密闭容器中反应2H2(g)+CO(g)?CH3OH(g) 达到平衡,下列说法正确的是( )
| 容器 | 温度/℃ | 物质的起始浓度/mol•L-1 | 物质的平衡浓度/mol•L-1 | ||
| c(H2) | c(CO) | c(CH3OH) | c(CH3OH) | ||
| Ⅰ | 400 | 0.20 | 0.10 | 0 | 0.080 |
| Ⅱ | 400 | 0.40 | 0.20 | 0 | |
| Ⅲ | 500 | 0 | 0 | 0.10 | 0.025 |
| A. | 该方应的正反应放热 | |
| B. | 达到平衡时,容器Ⅰ中反应物转化率比容器Ⅱ中的大 | |
| C. | 达到平衡时,容器Ⅱ中c(H2)大于容器Ⅲ中c(H2)的两倍 | |
| D. | 达到平衡时,容器Ⅲ中的反应速率比容器Ⅰ中的大 |
10.下列物质的除杂方案正确的是( )
| 选项 | 被提纯的物质 | 杂质 | 除杂试剂 | 除杂方法 |
| A | Cl2 (g) | HCl(g) | 饱和NaCl溶液、浓硫酸 | 洗气 |
| B | Na2CO3(aq) | NaHCO3(aq) | 过量NaOH溶液 | 洗液 |
| C | 铁粉(s) | 铝粉(s) | 过量NaOH溶液 | 过滤 |
| D | FeCl3(aq) | AlCl3(aq) | 过量氨水 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
17.下列化工生产过程中,未涉及氧化还原反应的是( )
| A. | 海带提碘 | B. | 氯碱工业 | C. | 氨碱法制碱 | D. | 海水提溴 |
1.下列说法错误的是( )
| A. | 各能级的原子轨道数按s、p、d、f的顺序分别为1、3、5、7 | |
| B. | N原子的轨道表示式: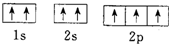 违反了泡利不相容原理 违反了泡利不相容原理 | |
| C. | 电子排布式(21Sc)1s22s22p63s23p63d3违反了能量最低原理 | |
| D. | 电子排布式(23V)1s22s22p63s23p63d34s2违反了洪特规则 |
8.下列化学用语的表达正确的是( )
| A. | 原子核内有10个中子的氧原子:${\;}_{6}^{18}$O | |
| B. | 氯原子的结构示意图: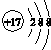 | |
| C. | Fe3+的最外层电子排布式为3s23p63d5 | |
| D. | 基态铜原子的外围电子排布图: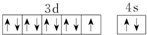 |
6.下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 溶液中加入HNO3无现象,再滴加BaCl2溶液 | 有白色沉淀生成 | 原溶液中有SO42- |
| B | AgI沉淀中滴入稀KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| C | 向溶液中加入少量KSCN溶液 | 有血红色溶液生成 | 溶液中含有Fe2+ |
| D | 向硫酸铜溶液中持续滴加氨水溶液 | 先有蓝色沉淀生成后溶解 | 氢氧化铜发生反应生成了[Cu(NH3)4]2+离子 |
| A. | A | B. | B | C. | C | D. | D |
 ;ZX2的化学式是SiO2.
;ZX2的化学式是SiO2.