题目内容
5.含氮的化合物在化学反应中变化复杂.现用如图所示仪器(夹持装置己省略及药品,探究亚硝酸钠与硫酸反应及气体产物的成分.已知:①NO+NO2+2OH-═2NO2-+H2O,②气体液化的温度:NO2 21℃、NO-152℃
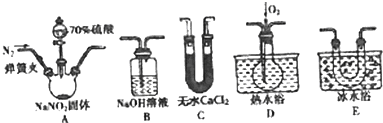
(1)为了检验装置A中生成的气体产物,上述仪器的连接顺序(按左→右连接)为ACEDB
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是:防止可能生成的NO被完全氧化成NO2,造成对A中反应气体产物检验的干扰.
(3)在关闭弹簧夹,滴入70%硫酸后,A中产生红棕色气体.
①盛装70%浓硫酸的仪器名称是分液漏斗.
②实验确认有NO的现象是D中刚开始为无色,通入O2后变为红棕色.
(4)通过上述实验探究过程,可得出装置A中反应的化学方程式是2NaNO2+H2SO4(浓)=Na2SO4+NO↑+NO2↑+H2O.
分析 (1)根据各部分装置的作用进行连接,C吸收水蒸气,B尾气处理,防止污染空气,D检验NO,E冷却二氧化氮;
(2)NO很容易被氧气氧化,装置中有空气,无法检验有NO生成;
(3)①依据图象和作用判断盛浓硫酸的仪器;
②根据一氧化氮和氧气反应生成红棕色二氧化氮气体判断,温度低于二氧化氮液化温度时,二氧化氮变成液态;
(4)根据反应物和生成物写出反应方程式,该反应中生成二氧化氮、一氧化氮,同时还有硫酸钠、水生成.
解答 解:(1)C吸收水蒸气,B尾气处理,防止污染空气,D检验NO,E冷却二氧化氮,利用D检验NO,所以装置的连接为A→C→E→D→B,故答案为:ACEDB;
(2)NO很容易被氧气氧化,装置中有空气,无法检验有NO生成,所以通氮气的目的是排尽整个装置中的空气,防止产生的NO被氧化生成NO2,
故答案为:防止可能生成的NO被完全氧化成NO2,造成对A中反应气体产物检验的干扰;
(3)①盛装70%浓硫酸的仪器名称是分液漏斗,
故答案为:分液漏斗;
②D中刚开始为无色,通入O2后变为红棕色,D中无色气体变成红色,说明含有NO气体,
故答案为:D中刚开始为无色,通入O2后变为红棕色;
(4)通过以上分析知,该反应中生成二氧化氮、一氧化氮,同时还有硫酸钠、水生成,所以反应方程式为2NaNO2+H2SO4=Na2SO4+NO2↑+NO↑+H2O,
故答案为:2NaNO2+H2SO4=Na2SO4+NO2↑+NO↑+H2O.
点评 本题考查实验方案设计,明确物质的性质和实验原理是解本题关键,注意实验设计要遵循严密性、可行性、科学性的原则,题目难度中等.

练习册系列答案
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案
相关题目
1.能形成XY2共价化合物的元素X和Y,其原子最外层电子排布是( )
| A. | 3s2和3s23p5 | B. | 2s22p2和2s22p4 | C. | 1s1和3s23p4 | D. | 3s23p4和2s22p4 |
2.合成导电高分子化合物PPV的反应为:
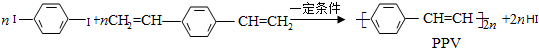
下列说法正确的是( )
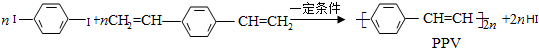
下列说法正确的是( )
| A. | PPV是聚苯乙炔 | |
| B. | 该反应为缩聚反应 | |
| C. | PPV与聚苯乙烯的最小结构单元组成相同 | |
| D. | 1 mol 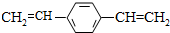 最多可与2 mol H2发生反应 最多可与2 mol H2发生反应 |
13.同周期的X、Y、Z三种元素,已知它们的最高价氧化物对应的水化物是HXO4、H2YO4、H3ZO4,则下列判断正确的是( )
| A. | 含氧酸的酸性:H3ZO4>H2YO4>HXO4 | |
| B. | 原子半径:Z>Y>X | |
| C. | 气态氢化物的稳定性按X、Y、Z顺序由弱到强 | |
| D. | 元素的负化合价的绝对值按X、Y、Z顺序由小到大 |
17.下列物质不能导电但属于电解质的是( )
| A. | 熔融的氯化镁 | B. | 饱和食盐水 | C. | 固态二氧化碳 | D. | 液态氯化氢 |
14.下列表示电子式的形成过程正确的是( )
| A. | 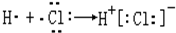 | B. | 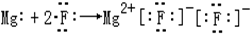 | ||
| C. | 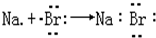 | D. | 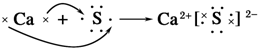 |
 ,X属于共价化合物.
,X属于共价化合物. .
.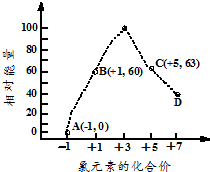 填写下列空白:
填写下列空白: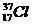 .
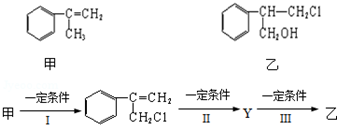
.
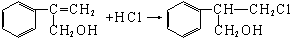 .
.