题目内容
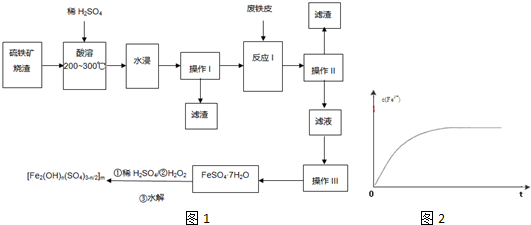
某厂以重晶石(有效成分是BaSO4)为主要原料制取Ba(OH)2?8H2O晶体的示意图如下:
已知:i.BaSO4(s)+2C(s)=2CO2(g)+BaS(s)△H1=+226.2 kJ/mol
C(s)+CO2(g)=2CO(g)△H2=+172.5kJ/mol
ii.某些物质的溶解度(g/100g)简表
回答下列 问题:
(1)炭与重晶石直接反应的热化学方程式是:BaSO4(s)+4C(s)=BaS(s)+4CO(g)△H= kJ/mol.
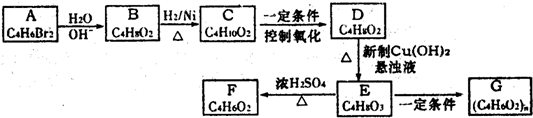
(2)由BaCl2溶液可通过不同途径得到Ba(OH)2?8H2O.
途径1:

①得到固体1的离子方程式是 . ②固体2与水反应的化学方程式是 .
途径2:

途径2中的“操作”是加热浓缩,冷却结晶,过滤.依据上述溶解度简表分析,过滤时的最佳温度是 ;能从混合液中得到Ba(OH)2?8H2O晶体的原因是 .
(3)若向滤液1中加入CuO粉末,可直接得到含Ba(OH)2?8H2O晶体和CuS的浊液,反应化学方程式是 .
将该浊液加热到80℃左右浓缩,趁热过滤,冷却滤液至室温,再过滤,即可得到Ba(OH)2?8H2O晶体.上述操作中趁热过滤的原因是 .

已知:i.BaSO4(s)+2C(s)=2CO2(g)+BaS(s)△H1=+226.2 kJ/mol
C(s)+CO2(g)=2CO(g)△H2=+172.5kJ/mol
ii.某些物质的溶解度(g/100g)简表
| 10℃ | 20℃ | 40℃ | 60℃ | 80℃ | |
| Ba(OH)2?8H2O | 2.48 | 3.89 | 8.22 | 20.9 | 101 |
| NaOH | 98.0 | 109 | 129 | 174 | 314 |
| NaCl | 35.8 | 35.9 | 36.4 | 37.1 | 38.0 |
| BaCl2 | 33.5 | 35.8 | 40.8 | 46.2 | 52.5 |
(1)炭与重晶石直接反应的热化学方程式是:BaSO4(s)+4C(s)=BaS(s)+4CO(g)△H=
(2)由BaCl2溶液可通过不同途径得到Ba(OH)2?8H2O.
途径1:

①得到固体1的离子方程式是
途径2:

途径2中的“操作”是加热浓缩,冷却结晶,过滤.依据上述溶解度简表分析,过滤时的最佳温度是
(3)若向滤液1中加入CuO粉末,可直接得到含Ba(OH)2?8H2O晶体和CuS的浊液,反应化学方程式是
将该浊液加热到80℃左右浓缩,趁热过滤,冷却滤液至室温,再过滤,即可得到Ba(OH)2?8H2O晶体.上述操作中趁热过滤的原因是
考点:物质分离和提纯的方法和基本操作综合应用,物质分离、提纯的实验方案设计
专题:实验设计题
分析:(1)①BaSO4(s)+2C(s)=2CO2(g)+BaS(s)△H1=+226.2 kJ/mol
②C(s)+CO2(g)=2CO(g)△H2=+172.5kJ/mol,
则由盖斯定律可知①+②×4得到BaSO4(s)+4C(s)=BaS(s)+4CO(g);
(2)途径1中氯化钡与碳酸钠反应生成碳酸钡沉淀,碳酸钡灼烧生成BaO,与水反应生成Ba(OH)2?8H2O;
途径2中,由溶解性表可知,较低温度时Ba(OH)2?8H2O易析出,且四种物质中相同温度时Ba(OH)2?8H2O的溶解度最小易得到;
(3)滤液1中加入CuO粉末,可直接得到含Ba(OH)2?8H2O晶体和CuS的浊液,则由反应物与生成物书写化学反应;该浊液加热到80℃左右浓缩,趁热过滤,减少晶体的损失.
②C(s)+CO2(g)=2CO(g)△H2=+172.5kJ/mol,
则由盖斯定律可知①+②×4得到BaSO4(s)+4C(s)=BaS(s)+4CO(g);
(2)途径1中氯化钡与碳酸钠反应生成碳酸钡沉淀,碳酸钡灼烧生成BaO,与水反应生成Ba(OH)2?8H2O;
途径2中,由溶解性表可知,较低温度时Ba(OH)2?8H2O易析出,且四种物质中相同温度时Ba(OH)2?8H2O的溶解度最小易得到;
(3)滤液1中加入CuO粉末,可直接得到含Ba(OH)2?8H2O晶体和CuS的浊液,则由反应物与生成物书写化学反应;该浊液加热到80℃左右浓缩,趁热过滤,减少晶体的损失.
解答:
解:(1)①BaSO4(s)+2C(s)=2CO2(g)+BaS(s)△H1=+226.2 kJ/mol
②C(s)+CO2(g)=2CO(g)△H2=+172.5kJ/mol,
则由盖斯定律可知①+②×4得到BaSO4(s)+4C(s)=BaS(s)+4CO(g),
△H=+226.2 kJ/mol+4×(+172.5kJ/mol)=+571.2kJ/mol,
故答案为:+571.2;
(2)途径1中氯化钡与碳酸钠反应生成碳酸钡沉淀,则得到固体1的离子方程式是CO32-+Ba2+=BaCO3↓,碳酸钡灼烧生成BaO,与水反应生成Ba(OH)2?8H2O,则固体2与水反应的化学方程式是BaO+9H2O=Ba(OH)2?8H2O;
途径2中,由溶解性表可知,较低温度时Ba(OH)2?8H2O易析出,且四种物质中相同温度时Ba(OH)2?8H2O的溶解度最小易得到,则过滤时的最佳温度是20℃或常温,因20℃时4种物质中Ba(OH)2?8H2O溶解度最小,
故答案为:CO32-+Ba2+=BaCO3↓;BaO+9H2O=Ba(OH)2?8H2O;20℃或常温;20℃时4种物质中Ba(OH)2?8H2O溶解度最小;
(3)滤液1中加入CuO粉末,可直接得到含Ba(OH)2?8H2O晶体和CuS的浊液,反应为BaS+CuO+9H2O=Ba(OH)2?8H2O+CuS,趁热过滤的原因是为减少过滤过程中Ba(OH)2?8H2O的损失,故答案为:BaS+CuO+9H2O=Ba(OH)2?8H2O+CuS;减少过滤过程中Ba(OH)2?8H2O的损失.
②C(s)+CO2(g)=2CO(g)△H2=+172.5kJ/mol,
则由盖斯定律可知①+②×4得到BaSO4(s)+4C(s)=BaS(s)+4CO(g),
△H=+226.2 kJ/mol+4×(+172.5kJ/mol)=+571.2kJ/mol,
故答案为:+571.2;
(2)途径1中氯化钡与碳酸钠反应生成碳酸钡沉淀,则得到固体1的离子方程式是CO32-+Ba2+=BaCO3↓,碳酸钡灼烧生成BaO,与水反应生成Ba(OH)2?8H2O,则固体2与水反应的化学方程式是BaO+9H2O=Ba(OH)2?8H2O;
途径2中,由溶解性表可知,较低温度时Ba(OH)2?8H2O易析出,且四种物质中相同温度时Ba(OH)2?8H2O的溶解度最小易得到,则过滤时的最佳温度是20℃或常温,因20℃时4种物质中Ba(OH)2?8H2O溶解度最小,
故答案为:CO32-+Ba2+=BaCO3↓;BaO+9H2O=Ba(OH)2?8H2O;20℃或常温;20℃时4种物质中Ba(OH)2?8H2O溶解度最小;
(3)滤液1中加入CuO粉末,可直接得到含Ba(OH)2?8H2O晶体和CuS的浊液,反应为BaS+CuO+9H2O=Ba(OH)2?8H2O+CuS,趁热过滤的原因是为减少过滤过程中Ba(OH)2?8H2O的损失,故答案为:BaS+CuO+9H2O=Ba(OH)2?8H2O+CuS;减少过滤过程中Ba(OH)2?8H2O的损失.
点评:本题考查物质分离提纯方法和综合应用,为高频考点,把握物质的性质、表格数据分析及混合物分离方法和原理为解答的关键,侧重分析与实验能力的考查,题目难度中等.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
用一定量的NH4NO3和KH2PO4的固体混合物可以配制无土栽培营养液,已知固体混合物中氮元素的质量分数为28%,则固体混合物中KH2PO4的质量分数为( )
| A、20% | B、25% |
| C、80% | D、85% |
在常温条件下,下列对醋酸的叙述中,不正确的是( )
| A、pH=5.6的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-) | ||
B、将pH=a的醋酸稀释为pH=a+1的过程中,
| ||
| C、浓度均为0.1mol?L-1的CH3COOH和CH3COONa溶液等体积混合后:c(CH3COO-)-c(CH3COOH)=2[c(H+)-c(OH-)] | ||
| D、等体积pH=a的醋酸与pH=b的NaOH溶液恰好中和时,存在a+b=14 |