题目内容
1.二甲醚是一种重要的化工原料,利用水煤气(CO、H2)合成二甲醚是工业上的常用方法,该方法由以下几步组成:2H2(g)+CO(g)?CH3OH(g)△H=-90.0kJ•mol-1 ①
2CH3OH(g?CH3OCH3(g)+H2O(g)△H=-24.5kJ•mol-1 ②
CO(g)+H2O(g)?CO2(g)+H2(g)△H=-41.1kJ•mol-1 ③
(1)反应①的△S<0(填“>”、“<”或“=”).在较高(填“较高”或“较低”)温度下该反应自发进行.
(2)在250℃的恒容密闭容器中,下列事实可以作为反应③已达平衡的是BC(填选项字母).
A.容器内气体密度保持不变 B.CO与CO2的物质的量之比保持不变
C.H2O与CO2的生成速率之比为1:1 D.该反应的平衡常数保持不变
(3)当合成气中CO与H2的物质的量之比恒定时,温度、压强对CO转化率的影响如图1所示.图1中A点的v(逆)<B点的v(正)(填“>”、“<”或“=”),说明理由B点对应的温度和压强都比A点高,温度升高,或压强增大,都会加快反应速率.实际工业生产中该合成反应的条件为500℃、4MPa请回答采用500℃的可能原因500℃时一氧化碳转化率较大,反应速率也较快.若温度过高,一氧化碳转化率降低,若温度过低,反应速率太慢.
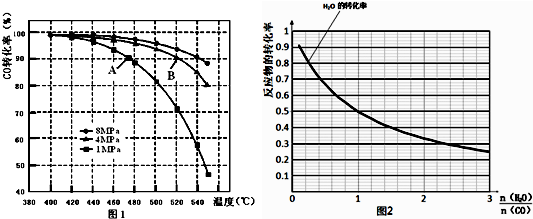
(4)一定温度下,密闭容器中发生反应③,水蒸气的转化率与n(H2O)∕n(CO)的关系如图2:计算该温度下反应③的平衡常数K=1.在图2中作出一氧化碳的转化率与n(H2O)∕n(CO)的曲线.
分析 (1)反应①的正反应为气体物质的量减小的反应,混乱度减小;△H-T△S<0反应自发进行;
(2)可逆反应到达平衡时,同种物质的正逆速率相等且保持不变,各组分的浓度、含量保持不变,由此衍生的其它一些量不变,判断平衡的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡;
(3)B点对应的温度和压强都比A点高,温度升高,或压强增大,都会加快反应速率;
500℃时一氧化碳转化率较大,反应速率也较快.若温度过高,一氧化碳转化率降低,若温度过低,反应速率太慢;
(4)由图可知,$\frac{n({H}_{2}O)}{n(CO)}$=1时水的转化率为0.5,令水、CO的起始物质的量均为1mol,转化的水为0.5mol,则:
CO(g)+H2O(g)?CO2(g)+H2(g)
起始量(mol):1 1 0 0
变化量(mol):0.5 0.5 0.5 0.5
平衡量(mol):0.5 0.5 0.5 0.5
由于反应前后气体物质的量不变,用物质的量代替浓度代入K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$计算平衡常数;
$\frac{n({H}_{2}O)}{n(CO)}$越大CO的转化率越大,$\frac{n({H}_{2}O)}{n(CO)}$=1时,CO与水的转化率相等为50%.
解答 解:(1)反应①的正反应为气体物质的量减小的反应,混乱度减小,则△S<0,反应的焓变△H<0,而△H-T△S<0反应自发进行,故在较高温度下具有自发性,
故答案为:<;较高;
(2)A.混合气体总质量不变,容器容积不变,容器内气体密度始终保持不变,故A错误;
B.CO与CO2的物质的量之比保持不变,说明二者物质的量保持不变,反应到达平衡,故B正确;
C.H2O与CO2的生成速率之比为1:1,说明水的消耗速率与生成速率相等,反应到达平衡,故C正确;
D.一定温度下,平衡常数为单质,该反应的平衡常数保持不变,不能说明反应到达平衡,故D错误,
故选:BC;
(3)B点对应的温度和压强都比A点高,温度升高,或压强增大,都会加快反应速率,故A点的v(逆)<B点的v(正);
500℃时一氧化碳转化率较大,反应速率也较快,若温度过高,一氧化碳转化率降低,若温度过低,反应速率太慢,故选择500℃的温度,
故答案为:<;B点对应的温度和压强都比A点高,温度升高,或压强增大,都会加快反应速率;500℃时一氧化碳转化率较大,反应速率也较快.若温度过高,一氧化碳转化率降低,若温度过低,反应速率太慢;
(4)由图可知,$\frac{n({H}_{2}O)}{n(CO)}$=1时水的转化率为0.5,令水、CO的起始物质的量均为1mol,转化的水为0.5mol,则:
CO(g)+H2O(g)?CO2(g)+H2(g)
起始量(mol):1 1 0 0
变化量(mol):0.5 0.5 0.5 0.5
平衡量(mol):0.5 0.5 0.5 0.5
由于反应前后气体物质的量不变,用物质的量代替浓度计算平衡常数,则平衡常数K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$=$\frac{0.5×0.5}{0.5×0.5}$=1;
$\frac{n({H}_{2}O)}{n(CO)}$越大CO的转化率越大,$\frac{n({H}_{2}O)}{n(CO)}$=1时,CO与水的转化率相等为50%,一氧化碳的转化率与$\frac{n({H}_{2}O)}{n(CO)}$的曲线变化为: ,
,
故答案为:1; .
.
点评 本题考查化学计算与影响因素、化学平衡图象、平衡状态判断、化学平衡常数、反应自发性等,(3)中作图为易错点,学生容易忽略交点时时转化率问题.

 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案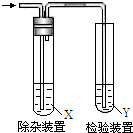 欲要检验不同条件下制得的乙烯,四个实验小组均用图所示装置对所制得的进行除杂、检验,所用试剂X、Y分别见下表所示.你认为设计中不需要除杂的小组是( )
欲要检验不同条件下制得的乙烯,四个实验小组均用图所示装置对所制得的进行除杂、检验,所用试剂X、Y分别见下表所示.你认为设计中不需要除杂的小组是( )| 小组 | 乙烯的制备 | 试剂X | 试剂Y |
| A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4 |
| B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
| C | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
| D | C2H5OH与浓硫酸加热至170℃ | NaOH溶液 | Br2的CCl4 |
| A. | A | B. | B | C. | C | D. | D |
| 容器 | 物质 | 起始浓度/(mol•L-1) | 平衡浓度/(mol•L-1) |
| Ⅰ | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| Ⅱ | N2O4 | 0 | 0.014 |
| NO2 | 0.100 | 0.072 |
| A. | 平衡时,Ⅰ、Ⅱ中反应物的转化率α(N2O4)<α(NO2) | |
| B. | 平衡时,升高温度,Ⅰ中速率减慢,Ⅱ中速率加快 | |
| C. | 当密度不变时,上述反应即达平衡 | |
| D. | 平衡后,升高温度,Ⅰ、Ⅱ中气体颜色都将变深 |
| A. | Na与水反应时增大水的用量 | |
| B. | Fe与稀硫酸反应制取H2 时,改用浓硫酸 | |
| C. | 在K2SO4与BaCl2两溶液反应时,降低温度 | |
| D. | Al与氧气燃烧生成Al2O3,将Al片改为Al粉, |
| A. | 过量的铁丝在氯气燃烧 | B. | 过量的铁粉与溴水反应 | ||
| C. | 烧碱溶液吸收NO2 | D. | 硝酸铜受热分解 |
| A. | 白色沉淀 | B. | 液体分层 | C. | 无明显现象 | D. | 黄绿色气体 |
| A. | 淀粉水解的最终产物是葡萄糖 | |
| B. | 重结晶法提纯苯甲酸时,为除去杂质和防止苯甲酸析出,应该趁热过滤 | |
| C. | 盐析可提纯蛋白质并能保持蛋白质的生理活性 | |
| D. | 油脂都不能使溴水褪色 |
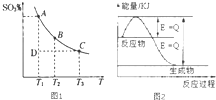 运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.
运用化学反应原理研究氮、硫、氯、碘等单质及其化合物的反应有重要意义.