题目内容
6.下列反应的产物中,只存在+3价铁元素或氮元素的是( )| A. | 过量的铁丝在氯气燃烧 | B. | 过量的铁粉与溴水反应 | ||
| C. | 烧碱溶液吸收NO2 | D. | 硝酸铜受热分解 |
分析 A.氯气具有强氧化性,和变价金属反应生成高价化合物;
B.过量铁粉和溴水反应生成溴化亚铁;
C.烧碱吸收二氧化氮反应生成亚硝酸钠、硝酸钠和水;
D.硝酸铜受热分解生成氧化铜二氧化氮和水;
解答 解:A.过量的铁丝在氯气燃烧生成氯化铁,2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3,故A符合;
B.过量铁粉和溴水反应生成溴化铁,2Fe+3Br2=2FeBr3,过量的铁和溴化铁溶液反应生成溴化亚铁,2FeBr3+Fe=3FeBr2,溶液中可能存在+2价和+3价的铁元素,故B不符合;
C.烧碱溶液吸收NO2 发生反应生成硝酸钠、亚硝酸钠和水,2NO2+2NaOH=NaNO2+NaNO3+H2O,产物中氮元素存在+2价和+3价,故C不符合;
D.硝酸铜受热分解生成氧化铜二氧化氮和水,2Cu(NO3)2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+4NO2↑+O2↑,但元素化合价为+4价,故D不符合;
故选A.
点评 本题考查了铁及其化合物性质的分析,主要是物质性质的掌握,掌握基础是关键,题目难度中等.

练习册系列答案
相关题目
16.下列关于常见有机物的说法不正确的是( )
| A. | C5H12属于烷烃且有三种同分异构体 | |
| B. | 乙酸、葡萄糖在一定条件下均能与Cu(OH)2反应 | |
| C. | 苯与浓硝酸、浓硫酸混合共热制取硝酸苯是发生取代反应 | |
| D. | 淀粉和纤维素均可用(C6H10O5)n表示,因此它们互为同分异构体 |
14.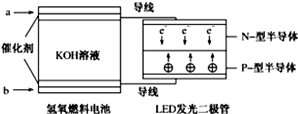 下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )
下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )
 下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )
下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )| A. | 氢氧燃料电池中OH-向b极移动 | |
| B. | 该装置中只涉及两种形式的能量转化 | |
| C. | H2在负极发生氧化反应 | |
| D. | P一型半导体连接电池负极 |
11.80°C,0.1mol/L NaHB溶液中c(H+)>c(OH-),可能正确的关系是( )
| A. | c(Na+)+c(H+)=c(HB-)+2c(B2-) | B. | 溶液的pH=1 | ||
| C. | c(H+)?c(OH-)=10-14 | D. | c(Na+)=c(H2B)+c(HB-) |
15.下列气体为红棕色的是( )
| A. | NO2 | B. | NO | C. | SO2 | D. | N2 |
16.下列物质中,既能与盐酸又能与氢氧化钠溶液反应,且有气体生成的是( )
| A. | Si | B. | SiO2 | C. | Al | D. | Al2O3 |
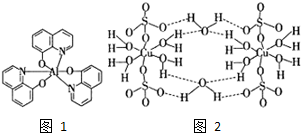 2012年10月1日起,我国将逐步淘汰白炽灯而采用高效照明的电致发光产品,电致发光材料有掺杂Mn2+和Cu2+的硫化锌、蒽单晶、8一羟基喹啉铝等.
2012年10月1日起,我国将逐步淘汰白炽灯而采用高效照明的电致发光产品,电致发光材料有掺杂Mn2+和Cu2+的硫化锌、蒽单晶、8一羟基喹啉铝等.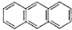 ,平面结构)属于非极性(填“极性”或“非极性”)分子.
,平面结构)属于非极性(填“极性”或“非极性”)分子.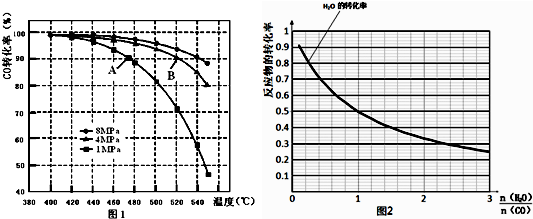
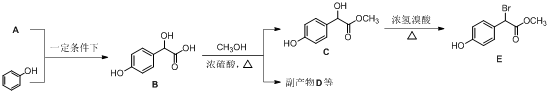
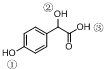 中①、②、③3个-OH的酸性由强到弱的顺序为③>①>②;写出B与过量Na2CO3溶液反应的化学方程式
中①、②、③3个-OH的酸性由强到弱的顺序为③>①>②;写出B与过量Na2CO3溶液反应的化学方程式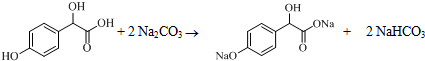 .
.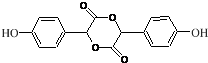 .
.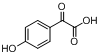 ,写出对应各步反应中依次所需的试剂和反应条件NaOH溶液;Cu、O2、加热;盐酸溶液.
,写出对应各步反应中依次所需的试剂和反应条件NaOH溶液;Cu、O2、加热;盐酸溶液.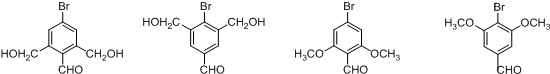 (不考虑立体异构).
(不考虑立体异构).