题目内容
13.向饱和食盐水中滴加一定量浓盐酸,对出现现象的预测可能正确的是( )| A. | 白色沉淀 | B. | 液体分层 | C. | 无明显现象 | D. | 黄绿色气体 |
分析 饱和氯化钠溶液中存在溶解平衡NaCl(s)?Na+(l)+Cl-(l),加入浓盐酸后氯离子浓度增大,则溶解平衡向着逆向移动,导致析出氯化钠晶体,据此进行解答.
解答 解:饱和氯化钠溶液中存在溶解平衡:NaCl(s)?Na+(l)+Cl-(l),
由于加入浓盐酸,溶液中氯离子浓度增大,抑制了氯化钠的溶解,会析出白色的NaCl晶体,
故选A.
点评 本题考查了饱和溶液中溶解平衡及其影响,题目难度不大,明确溶解平衡及其影响为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
4.设阿伏加德罗常数为NA,下列说法中正确的是( )
| A. | 标准状况下,2.24L水含有0.1NA个水分子 | |
| B. | 0.3molSO2中含有的氧原子数为0.3NA | |
| C. | 标准状况下,22.4L氖气含有2NA个原子 | |
| D. | 1L 0.1mol/LMgCl2溶液中含Cl-数为0.2NA |
8.有机物M的结构如图所示.关于M的描述正确的是( )
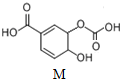

| A. | 分子式为C8H6O6 | |
| B. | 能发生中和、取代、消去、氧化、加成反应 | |
| C. | 1molM与溴水发生反应的产物可能有3种 | |
| D. | 1molM与足量氢氧化钠溶液反应,消耗4molNaOH |
5.下列说法不正确的是( )
| A. | 同系物的化学性质相似 | |
| B. | 甲烷、乙烷互为同系物 | |
| C. | 分子式相同,结构不同的化合物互称为同分异构体 | |
| D. | 同分异构体之间的转化属于物理变化 |
2.下列离子方程式正确的是( )
| A. | Zn与稀H2SO4反应:Zn+2H+═Zn2++H2↑ | |
| B. | 铁和稀硝酸反应:Fe+2H+═Fe2++H2↑ | |
| C. | Cl2与NaOH溶液反应:Cl2+2OH-═2Cl-+H2O | |
| D. | 碳酸钙溶于盐酸:CO32-+2H+═CO2↑+H2O |
3. 如图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是( )
如图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是( )
 如图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是( )
如图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是( )| A. | 31d和33d属于同种核素 | B. | 气态氢化物的稳定性:a>d>e | ||
| C. | 工业上常用电解法制备单质b和c | D. | a和b形成的化合物不可能含共价键 |
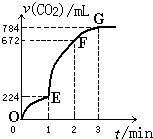 常温下,用纯净的CaCO3与100mL稀盐酸制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况).
常温下,用纯净的CaCO3与100mL稀盐酸制取CO2,实验过程记录如图所示(CO2的体积已折算为标准状况).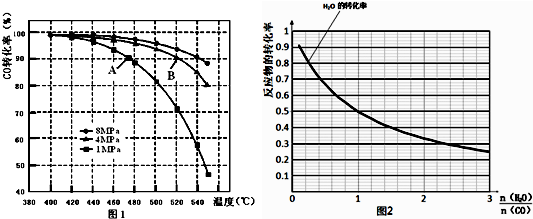
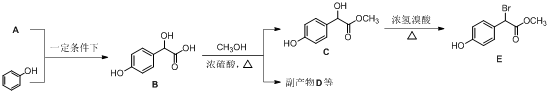
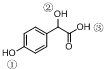 中①、②、③3个-OH的酸性由强到弱的顺序为③>①>②;写出B与过量Na2CO3溶液反应的化学方程式
中①、②、③3个-OH的酸性由强到弱的顺序为③>①>②;写出B与过量Na2CO3溶液反应的化学方程式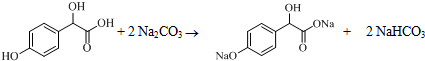 .
.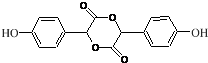 .
.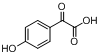 ,写出对应各步反应中依次所需的试剂和反应条件NaOH溶液;Cu、O2、加热;盐酸溶液.
,写出对应各步反应中依次所需的试剂和反应条件NaOH溶液;Cu、O2、加热;盐酸溶液.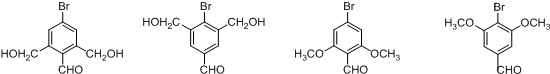 (不考虑立体异构).
(不考虑立体异构).