题目内容
9.下列措施对增大反应速率明显有效的是( )| A. | Na与水反应时增大水的用量 | |
| B. | Fe与稀硫酸反应制取H2 时,改用浓硫酸 | |
| C. | 在K2SO4与BaCl2两溶液反应时,降低温度 | |
| D. | Al与氧气燃烧生成Al2O3,将Al片改为Al粉, |
分析 A、钠与水反应剧烈,加水不能改变浓度;
B、浓硫酸具有强氧化性,使铁发生钝化;
C、降低温度,反应速率减慢;
D、压强只对气体的反应速率有影响,对非气体的反应没有影响,增大压强速率不变.
解答 解:A、加水不能改变浓度水的浓度,对反应速率没有影响,故A错误;
B、浓硫酸具有强氧化性,与铁发生钝化反应,没有氢气生成,不能提高生成气体的反应速率,故B错误;
C、在K2SO4与BaCl2两溶液反应时,降低温度,反应速率减慢,故C错误;
D、将Al片改成Al粉,增大了反应物的接触面积,所以能使反应速率加快,故D正确;
故选:D.
点评 本题考查化学反应速率的影响因素,题目难度不大,注意浓硫酸与稀硫酸的性质的不同,为本题的易错点.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.设阿伏加德罗常数为NA,下列说法中正确的是( )
| A. | 标准状况下,2.24L水含有0.1NA个水分子 | |
| B. | 0.3molSO2中含有的氧原子数为0.3NA | |
| C. | 标准状况下,22.4L氖气含有2NA个原子 | |
| D. | 1L 0.1mol/LMgCl2溶液中含Cl-数为0.2NA |
14.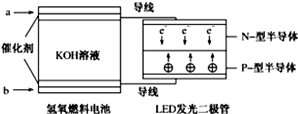 下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )
下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )
 下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )
下图是氢氧燃料电池驱动LED发光的装置,其电极反应式为:2H2+4OH--4e-═4H2O,O2+2H2O+4e-═4OH-.下列有关叙述正确的是( )| A. | 氢氧燃料电池中OH-向b极移动 | |
| B. | 该装置中只涉及两种形式的能量转化 | |
| C. | H2在负极发生氧化反应 | |
| D. | P一型半导体连接电池负极 |
19.下列物质属于电解质且能导电的是( )
| A. | 金属铜 | B. | 碳酸钠晶体 | C. | 硝酸钠溶液 | D. | 熔融氯化钠 |
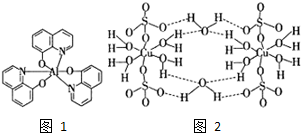 2012年10月1日起,我国将逐步淘汰白炽灯而采用高效照明的电致发光产品,电致发光材料有掺杂Mn2+和Cu2+的硫化锌、蒽单晶、8一羟基喹啉铝等.
2012年10月1日起,我国将逐步淘汰白炽灯而采用高效照明的电致发光产品,电致发光材料有掺杂Mn2+和Cu2+的硫化锌、蒽单晶、8一羟基喹啉铝等.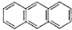 ,平面结构)属于非极性(填“极性”或“非极性”)分子.
,平面结构)属于非极性(填“极性”或“非极性”)分子.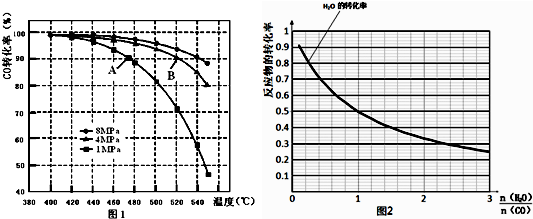
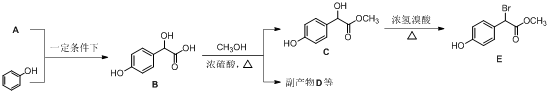
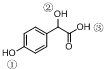 中①、②、③3个-OH的酸性由强到弱的顺序为③>①>②;写出B与过量Na2CO3溶液反应的化学方程式
中①、②、③3个-OH的酸性由强到弱的顺序为③>①>②;写出B与过量Na2CO3溶液反应的化学方程式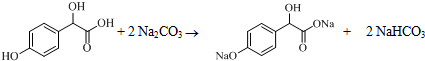 .
.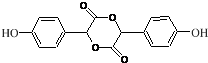 .
.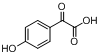 ,写出对应各步反应中依次所需的试剂和反应条件NaOH溶液;Cu、O2、加热;盐酸溶液.
,写出对应各步反应中依次所需的试剂和反应条件NaOH溶液;Cu、O2、加热;盐酸溶液.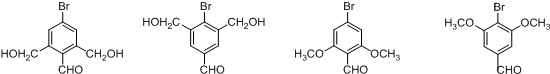 (不考虑立体异构).
(不考虑立体异构).