题目内容
18.能说明氯元素的非金属性比硫元素强的事实是( )①Cl2与H2S溶液发生置换反应
②受热时H2S能分解,HCl则不能
③单质硫可在空气中燃烧,Cl2不能
④HCl是强酸,H2S是弱酸.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
分析 根据非金属元素对应离子的还原性、气态氢化物的稳定性、最高价氧化物水化物的酸性、单质之间的置换反应等来比较非金属性,以此来解答.
解答 解:①Cl2与H2S溶液发生置换反应,则非金属性Cl>S,能说明氯元素的非金属性比硫元素强,故正确;
②元素的非金属性越强,对应的氢化物越稳定,受热时H2S能分解,HCl则不能,则非金属性Cl>S,能说明氯元素的非金属性比硫元素强,故正确;
③单质硫可在空气中燃烧,Cl2不能,体现的是单质的还原性强弱,不能证明元素的非金属性强弱,故错误;
④最高价含氧酸的酸性强,则元素的非金属性弱,只有根据HClO4的酸性比H2SO4的强,才得到非金属性Cl>S,才能说明氯元素的非金属性比硫元素强,故错误;
故选A.
点评 本题考查非金属性的比较,明确常见的比较方法是解答本题的关键,注重知识的归纳总结,题目难度不大.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
13.符合下列条件的烃的衍生物的结构共有(不考虑立体异构)( )
①分子式符合CxH2x+2Oy
②相对分子质量介于70-100之间
③氧元素的质量分数为18.18%
④分子中含有2个甲基
⑤属于醇类.
①分子式符合CxH2x+2Oy
②相对分子质量介于70-100之间
③氧元素的质量分数为18.18%
④分子中含有2个甲基
⑤属于醇类.
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
3.由甲醛、乙炔和苯组成的混合物中,测得含碳元素的质量分数为72%,则混合物中氢元素的质量分数为( )
| A. | 20.7% | B. | 22% | C. | 1.3% | D. | 7.3% |
10.下列实验中,对应的现象及结论都正确且存在因果关系的是( )
| 选项 | 实验 | 现象 | 结论 |
| A | 用酒精灯加热摩尔盐(NH4)2Fe(SO4)2•6H2O,产生的气体通过装有无水硫酸铜的干燥管 | 干燥管中的白色粉末先变成天蓝色,后又变成深蓝色 | 加热温度较低时摩尔盐分解产生水蒸气,温度稍高时分解产物中有氨气 |
| B | 向某溶液中滴加BaCl2溶液,随后加稀硝酸酸化 | 溶液中产生白色沉淀,加稀硝酸不溶解 | 原溶液中一定含有SO42- |
| C | 向CuSO4溶液中通入H2S气体 | 溶液的蓝色褪去,生成黑色沉淀 | 氢硫酸的酸性比硫酸强 |
| D | 向2ml0.1mol/LAgNO3溶液中先滴几滴0.1mol/L的NaCl溶液,再滴入几滴0.1mol/L的NaI溶液 | 先生成白色沉淀,后生成黄色沉淀 | 溶度积KSp(AgCl) >KSp(AgI) |
| A. | A | B. | B | C. | C | D. | D |
7.在氯水中存在多种分子和离子,它们在不同的反应中表现各自的性质.下列现象与结论相等的是( )
| A. | 溶液呈黄绿色,且具有刺激性气味,说明Cl2的存在 | |
| B. | 加入有色布条,有色布条褪色,说明溶液中有Cl2存在 | |
| C. | 加入NaHCO3溶液,有无色气体产生,说明有HClO存在 | |
| D. | 先加入盐酸酸化,再加AgNO3溶液产生白色沉淀,说明有Cl-存在 |
8.生活中处处有化学,下列表述不正确的是( )
| A. | 福尔马林可作食品的保鲜剂 | |
| B. | 聚乙烯塑料制品可作食品的包装材料 | |
| C. | 碳酸氢钠可于治疗胃酸过多症 | |
| D. | 食盐可作调味剂,也可作食品防腐剂 |
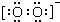 ;
; .
. CF4
CF4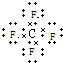 BaCl2
BaCl2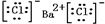 N2
N2 CO2
CO2 .
.