题目内容
9.按要求填空:(1)S2-离子的结构示意图
 .
.(2)质量数为23,中子数为12的原子的原子符号是${\;}_{11}^{23}Na$(用${\;}_Z^AX$的形式表示).
(3)现有A、B、C三种微粒,A微粒有两层电子,最外层电子数为4;B微粒第二层电子数是最内层电子数的三倍;C微粒质子数为11,带一个单位正电荷.
①分别写出各个微粒的符号AC;BO;CNa+.
②A、B、C所属元素两个或三个组合,可以形成哪些化合物,任意写三种CO、CO2、Na2O.
分析 (1)硫离子的核电荷数为16,核外电子总数为18,最外层含有8个电子,据此画出硫离子的离子结构示意图;
(2)质量数为23,中子数为12的原子Na,根据其质子数和电子数画出原子结构示意图;
(3)A微粒有两层电子,最外层电子数为4,故A为原子,且核外共有6个电子,故为C原子;B微粒第二层电子数是最内层电子数的三倍,故B只能有2个电子层,且最外层有6个电子,故为O原子;C微粒质子数为11,带一个单位正电荷,故C为钠离子.据此分析.
解答 解:(1)硫离子核外存在18个电子,核内有16个质子,最外层达到8电子稳定结构,其离子结构示意图为: ,
,
故答案为: ;
;
(2)质量数为23,中子数为12的原子Na,其质子数为11和电子数为11,故为质量数为23的一种钠原子,故原子符号为${\;}_{11}^{23}Na$,故答案为:${\;}_{11}^{23}Na$;
(3)A微粒有两层电子,最外层电子数为4,故A为原子,且核外共有6个电子,故为C原子;B微粒第二层电子数是最内层电子数的三倍,故B只能有2个电子层,且最外层有6个电子,故为O原子;C微粒质子数为11,带一个单位正电荷,故C为钠离子.
①A为C,B为O,C为Na+,故答案为:C、O、Na+;②;
②A、B、C所属元素分别为C元素、O元素和Na元素,故形成的化合物可以是CO或CO2或Na2O,故答案为:CO或CO2或Na2O;
点评 本题考查了离子结构示意图的书写、原子符号的表示等,题目难度不大,明确粒子结构示意图的表示方法为解答关键,试题侧重 基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案
相关题目
19.某1.6g有机物燃烧后的产物先通过浓H2SO4,浓H2SO4增重3.6g,后又通过碱石灰、碱石灰增重4.4g,下列说法正确的是( )
| A. | 浓H2SO4增重的是CO2的质量 | B. | 该有机物中没有氧元素 | ||
| C. | 该有机物中有氧元素 | D. | 碱石灰增重的是CO2和H2O的质量 |
20.常温下,下列关于电解质溶液的说法正确的是( )
| A. | 将pH=4 CH3COOH溶液加水稀释10倍,溶液中各离子浓度均减小 | |
| B. | 用CH3COOH溶液滴定等浓度的NaOH溶液至pH=7,V(CH3COOH溶液)<V(NaOH溶液) | |
| C. | 向0.2 mol/L的盐酸溶液中加入等体积0.1 mol•L-1 NH3•H2O溶液:c(Cl-)=c(H+)+c( NH3•H2O) | |
| D. | 25℃时,0.1 mol•L-1的NaClO2溶液和0.001 mol•L-1CH3COONa溶液pH相等,则HClO2的电离平衡常数大于CH3COOH |
17.测得某无色透明溶液的pH=2,则在该溶液中能大量共存的离子是( )
| A. | Na+ Cl- Mg2+ SO42- | B. | K+ Cu2+ I- SO42- | ||
| C. | NO3- K+ Cl- OH- | D. | Al3+ Na+ S2- Cl- |
4.(1)分别用一种试剂将下列物质中混入的少量杂质除去(括号内为杂质)
(2)亚硫酸钠晶体易氧化变质,简述检验亚硫酸钠晶体是否变质的方法取少量亚硫酸钠晶体加蒸馏水溶解,滴入BaCl2溶液,再滴加足量盐酸,若还有白色沉淀,则晶体已变质.
| 物 质 | 加入试剂的化学式 | 有关离子方程式 |
| NaCl(Na2SO4) | ||
| FeCl2(FeCl3) | ||
| Na2CO3 溶液(NaHCO3) |
14.下列化合物中含有手性碳原子的是( )
| A. | CCl2F2 | B. | 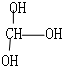 | C. | CH3CH2OH | D. | 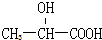 |
1.下列元素电负性最大的是( )
| A. | C | B. | F | C. | Cl | D. | N |
18.能说明氯元素的非金属性比硫元素强的事实是( )
①Cl2与H2S溶液发生置换反应
②受热时H2S能分解,HCl则不能
③单质硫可在空气中燃烧,Cl2不能
④HCl是强酸,H2S是弱酸.
①Cl2与H2S溶液发生置换反应
②受热时H2S能分解,HCl则不能
③单质硫可在空气中燃烧,Cl2不能
④HCl是强酸,H2S是弱酸.
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
19. 某反应历程,假设体系的始态为S,终态为L,它们之间的变化用两段弧线(可以包含着任意数目的中间步骤)连接如图所示.( )
某反应历程,假设体系的始态为S,终态为L,它们之间的变化用两段弧线(可以包含着任意数目的中间步骤)连接如图所示.( )
 某反应历程,假设体系的始态为S,终态为L,它们之间的变化用两段弧线(可以包含着任意数目的中间步骤)连接如图所示.( )
某反应历程,假设体系的始态为S,终态为L,它们之间的变化用两段弧线(可以包含着任意数目的中间步骤)连接如图所示.( )| A. | 一定有△H1<0 | B. | 一定有△H2<0 | ||
| C. | 一定有△H1<0,△H2>0 | D. | 一定有△H1+△H2=0 |