题目内容
20.以下是有关SO2、Cl2的性质实验.(1)某小组设计如图所示的装置图(图中夹持和加热装置略去),分别研究SO2和Cl2的性质.

若从左端分别通入SO2和Cl2,装置A中观察到的现象是否相同?相同(填“相同”或“不相同”); 若装置D中装的是五氧化二钒(催化剂),通入SO2时,打开K通入适量O2的化学反应方程式为2SO2+O2 $\frac{\underline{催化剂}}{△}$2SO3E中盛有NaOH 溶液.
(2)若装置B中装有5.0mL 1.0×10-3mol/L碘水,当通入足量Cl2完全反应后,共转移了5.0×10-5mol电子,该反应的化学方程式为5Cl2+I2+6H2O=2HIO3+10HCl.
(3)某同学将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量(填字母)AC,则可以看到白色沉淀产生.
A.氨水B.稀盐酸C.稀硝酸D.氯化钙.
分析 (1)①二氧化硫具有漂白性和有机色素结合为不稳定的化合物,氯气通入溶液中与水反应生成的次氯酸具有漂白性,可以氧化有机色素为无色;二氧化硫催化氧化为三氧化硫;E为尾气处理,吸收多余的SO2和Cl2应盛有氢氧化钠溶液;
(2)设碘元素在氧化产物中的化合价为a,则根据电子转移守恒有5.0×10-3L×1.0×10-3mol/L×2×a=5.0×10-5mol,解得:a=+5,所以碘单质被氧化为HIO3,据此书写方程式;
(3)足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量物质可以看到白色沉淀产生;
A.氨水和二氧化硫反应生成亚硫酸铵,亚硫酸根离子和钡离子结合生成沉淀;
B.稀盐酸不和二氧化硫反应不能生成沉淀;
C.稀硝酸溶液具有强氧化性,将二氧化硫氧化成硫酸根,结合钡离子生成沉淀;
D.氯化钙溶液和二氧化硫不反应.
解答 解:(1)①二氧化硫能和有色物质反应生成无色物质,所以二氧化硫有漂白性;氯气和水反应生成次氯酸,次氯酸具有强氧化性,能使有色物质褪色,所以若从左端分别通入SO2和Cl2,装置A中观察到的现象相同,都使品红褪色;二氧化硫和氧气在五氧化二钒作催化剂、加热条件下能发生氧化还原反应生成三氧化硫,反应方程式为 2SO2+O2 $\frac{\underline{催化剂}}{△}$2SO3,E为尾气处理,吸收多余的SO2和Cl2应盛有氢氧化钠溶液,
故答案为:相同;2SO2+O2 $\frac{\underline{催化剂}}{△}$2SO3;NaOH;
(2)若装置B中装有5.0mL 1.0×10-3mol/L的碘水,当通入足量Cl2完全反应后,转移的电子为5.0×10-5mol,令碘元素在氧化产物中的化合价为a,则根据电子转移守恒有5.0×10-3L×1.0×10-3mol/L×2×a=5.0×10-5mol,解得a=+5,所以碘单质被氧化为HIO3,则该反应的化学方程式为5Cl2+I2+6H2O=2HIO3+10HCl,
故答案为:5Cl2+I2+6H2O=2HIO3+10HCl;
(3)将足量的SO2通入一支装有氯化钡溶液的试管,未见沉淀生成,若向该试管中加入足量试剂仍然无法观察到沉淀产生,说明不发生反应:
A、氨水加入后生成亚硫酸铵,亚硫酸根和钡离子生成沉淀,故A正确;
B、稀盐酸加入后不反应,故B错误;
C、稀硝酸溶液具有强氧化性,将二氧化硫氧化成硫酸根,与钡离子生成硫酸钡沉淀,故C正确;
D.氯化钙溶液和二氧化硫不反应,故D错误;
故答案为:AC.
点评 本题考查了性质实验方案的设计,明确二氧化硫的性质是解本题关键,会根据二氧化硫的性质分析装置中各个装置的作用及发生的反应,注意稀硝酸有强氧化性而氧化二氧化硫,为易错点,题目难度中等.

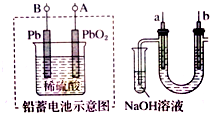
| A. | 铅蓄电池A极应与U形管中a极连接 | |
| B. | 铅蓄电池放电时溶液的pH值变小 | |
| C. | a电极用铁作电极,b电极用石墨作电极 | |
| D. | 实验结束后可将U型管、试管中的溶液倒入下水道 |
 利用下图装置可以进行实验并能达到实验目的是( )
利用下图装置可以进行实验并能达到实验目的是( )| 选项 | 实验目的 | 试剂X | 试剂Y |
| A | Na2SO3和盐酸制取并收集纯净干燥的SO2 | 饱和NaHSO3溶液 | 浓硫酸 |
| B | 用Cu与稀硝酸制取并收集纯净干燥的NO | 水 | 浓硫酸 |
| C | 苯与浓溴水在铁催化下反应制溴苯并收集HBr | CCl4 | 浓硫酸 |
| D | 用MnO2和浓盐酸制取并收集纯净干燥的Cl2 | 饱和食盐水 | 浓硫酸 |
| A. | A | B. | B | C. | C | D. | D |
| A. | NaOH溶液 | B. | AgNO3溶液 | C. | 溴水 | D. | 淀粉碘化钾溶液 |
| A. | 若A2和B2的总能量大于生成的AB的总能量,则反应放热 | |
| B. | 若A2和B2的总能量小于生成的AB的总能量,则反应放热 | |
| C. | 若该反应为放热反应,则Q1+Q2>Q3 | |
| D. | 若该反应为吸热反应,则Q1+Q2>Q3 |
| A. | v(A)=0.030 mol/(L•s) | B. | v(B)=0.075 mol/(L•s) | ||
| C. | v(C)=0.030 mol/(L•s) | D. | v(D)=0.030 mol/(L•s) |
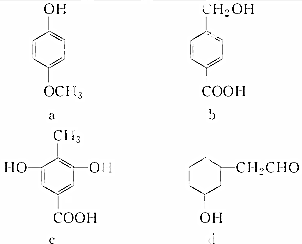
| A. | a属于酚类,可与NaHCO3溶液反应产生CO2 | |
| B. | b属于酚类,1 molb最多能与3 molH2发生加成反应 | |
| C. | 1 mol c最多能与3 mol Br2发生反应 | |
| D. | d属于醇类,可以发生消去反应 |
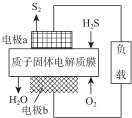 H2S废气资源化利用途径之一是回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g )═S2(s)+2H2O(l)△H=-632kJ•mol-1.图为质子膜H2S燃料电池的示意图.下列说法正确的是( )
H2S废气资源化利用途径之一是回收能量并得到单质硫.反应原理为:2H2S(g)+O2(g )═S2(s)+2H2O(l)△H=-632kJ•mol-1.图为质子膜H2S燃料电池的示意图.下列说法正确的是( )| A. | 电极a为电池的正极 | |
| B. | 电极 b 上发生的电极反应为:O2+4H++4e-═2H2O | |
| C. | 该装置是一种将热能转化为电能的装置 | |
| D. | H+经质子膜进入a极区 |
 ;反应类型加聚反应.
;反应类型加聚反应.