题目内容
8.三氯甲烷(CHCl3)又称氯仿,可用作麻醉剂,但在光照下易被氧化成剧毒的光气(COCl2).其反应式为2CHCl3+O2$\stackrel{光}{→}$2COCl2+2HCl,为了防止事故发生,在使用三氯甲烷前要先检验一下其是否变质,检验用的最佳试剂是( )| A. | NaOH溶液 | B. | AgNO3溶液 | C. | 溴水 | D. | 淀粉碘化钾溶液 |
分析 由2CHCl3+O2$\stackrel{光}{→}$2COCl2+2HCl可知,如果氯仿变质会生成HCl,可以通过检验是否有氯化氢生成判断氯仿是否变质,如加入AgNO3溶液生成AgCl白色沉淀,以此来解答.
解答 解:A.加入NaOH溶液,没有明显的现象,不能用来检验是否被氧化,故A错误;
B.氯仿被氧化时生成HCl,加入硝酸酸化的硝酸银溶液生成AgCl白色沉淀,可检验,故B正确;
C.氯化氢与与溴水不反应,无法检验氯仿是否变质,故C错误;
D.均与淀粉碘化钾不反应,不能用来检验,故D错误;
故选B.
点评 本题考查氯仿是否变质的实验设计,为高频考点,把握氯仿变质的方程式结合有关物质的性质进行判断为解答的关键,侧重分析与迁移应用能力的考查,题目难度不大.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案
相关题目
18.某有机化合物,只含碳、氢、氧三种元素中的两种或三种,相对分子质量为74,完全燃烧时产生等物质的量的CO2和H2O.它的分子式可能为( )
| A. | C4H10O | B. | C4H4O2 | C. | C3H6O2 | D. | C4H8O2 |
19. 下面是18×7的格子,按要求作答
下面是18×7的格子,按要求作答
(1)用封闭的实线绘出元素周期表的轮廓,注意:不得使用铅笔作图.
(2)C元素的一种中子数为10的同位素的原子符号为818O,C2-的离子结构示意图为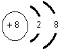 ,C、D、E、F的简单离子半径由小到大顺序是Al3+<Mg2+<F-<O2-.(填写离子符号 )
,C、D、E、F的简单离子半径由小到大顺序是Al3+<Mg2+<F-<O2-.(填写离子符号 )
(3)A、G、C中的2种或3种元素能形成18个电子的分子N2H4、H2O2(填化学式),其中A、G也能形成GA5的离子化合物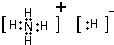 (填电子式).
(填电子式).
(4)请分别用1个离子方程式说明B和F的金属性强弱:Al3++3OH-=Al(OH)3↓或Al(OH)3+OH-=AlO2-+2H2O,C和D的非金属性强弱2F2+2H2O=4HF+O2.
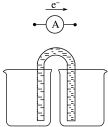
(5)Fe位于周期表第四周期VIII族,请运用原电池原理设计实验,验证Cu2+、Fe3+氧化性的强弱.写出总反应式:2 Fe3++Cu=2Fe2++Cu2+负极电极反应式:Cu-2e-=Cu2+,并在方框内画出实验装置图,并标注电极材料和电解质溶液.
 下面是18×7的格子,按要求作答
下面是18×7的格子,按要求作答| A | He | ||||||||||||||||
| G | C | D | |||||||||||||||
| B | E | F | I | H | |||||||||||||
| Fe | Cu | ||||||||||||||||
(2)C元素的一种中子数为10的同位素的原子符号为818O,C2-的离子结构示意图为
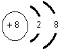 ,C、D、E、F的简单离子半径由小到大顺序是Al3+<Mg2+<F-<O2-.(填写离子符号 )
,C、D、E、F的简单离子半径由小到大顺序是Al3+<Mg2+<F-<O2-.(填写离子符号 )(3)A、G、C中的2种或3种元素能形成18个电子的分子N2H4、H2O2(填化学式),其中A、G也能形成GA5的离子化合物
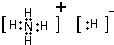 (填电子式).
(填电子式).(4)请分别用1个离子方程式说明B和F的金属性强弱:Al3++3OH-=Al(OH)3↓或Al(OH)3+OH-=AlO2-+2H2O,C和D的非金属性强弱2F2+2H2O=4HF+O2.
(5)Fe位于周期表第四周期VIII族,请运用原电池原理设计实验,验证Cu2+、Fe3+氧化性的强弱.写出总反应式:2 Fe3++Cu=2Fe2++Cu2+负极电极反应式:Cu-2e-=Cu2+,并在方框内画出实验装置图,并标注电极材料和电解质溶液.
17.下列各组中的性质比较,正确的是( )
①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
③还原性:Br->Cl->F-
④稳定性:HCl>H2S>PH3.
①酸性:HClO4>HBrO4>HIO4
②碱性:Ba(OH)2>Ca(OH)2>Mg(OH)2
③还原性:Br->Cl->F-
④稳定性:HCl>H2S>PH3.
| A. | 都正确 | B. | .①②③ | C. | .②③④ | D. | .①②④ |
18.下列说法正确的是( )
| A. | 邻二溴苯只有一种可以证明苯环结构中不存在单双键交替结构 | |
| B. | 可以用分液漏斗分离苯和硝基苯 | |
| C. | 制取一氯乙烷的最佳途径是通过乙烷与氯气反应获得 | |
| D. | 等物质的量的乙醇和水分别与足量的钠反应,生成的气体体积比为3:1 |
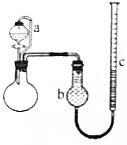 某研究性学习小组为了测定镀锌薄铁板(假设只含Fe和Zn)中锌的质量分数ω(Zn),用如图所示装置(夹持装置略去)进行实验,通过测定产生H2的体积计算ω(Zn).已知:①锌易溶于强碱溶液,发生反应为Zn+2NaOH═Na2ZnO2+H2↑.②所用的镀锌薄铁板均为m1g.回答下列问题:
某研究性学习小组为了测定镀锌薄铁板(假设只含Fe和Zn)中锌的质量分数ω(Zn),用如图所示装置(夹持装置略去)进行实验,通过测定产生H2的体积计算ω(Zn).已知:①锌易溶于强碱溶液,发生反应为Zn+2NaOH═Na2ZnO2+H2↑.②所用的镀锌薄铁板均为m1g.回答下列问题: .
.