题目内容
3.已知水在25℃和95℃时,其电离平衡曲线如图所示: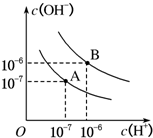
(1)则25℃时水的电离平衡曲线应为A (填“A”或“B”),请说明理由温度越高Kw越大
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则NaOH溶液与H2SO4溶液的体积比为10:1.
(3)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是pH1+pH2=14.
(4)曲线B对应温度下,pH=2的HCl溶液和pH=10的某BOH溶液等体积混合后,混合溶液的pH=8.请分析其原因:BOH为弱碱,c(BOH)?c(HCl),等体积混合两溶液时,BOH过量,混合溶液呈碱性.
分析 (1)水的电离是吸热反应,升高温度促进水电离,水中c(H+)、c(OH-)都增大;
(2)25℃时,将pH=9的NaOH溶液中c(OH-)=10-5 mol/L,pH=4的H2SO4溶液中c(H+)=10-4 mol/L,要使混合溶液呈中性,则n(OH-)=n(H+);
;
(3)99℃时,pH1=a的某强酸溶液中C(H+)=10-a mol/L,pH2=b的某强碱溶液C(OH-)=10b-12 mol/L,溶液呈中性,则酸中 n(H+)应等于碱中n(OH-);
(4)pH=3的盐酸溶液和pH=9的某碱溶液等体积混合后,氢离子和氢氧根离子恰好反应.
解答 解:(1)纯水中,水的电离是吸热反应,升高温度促进水电离,c(OH-)、c(H+)增大且c(OH-)=c(H+),水的离子积常数增大,所以25℃时水的电离平衡曲线应为A,故答案为:A;温度越高Kw越大;
(2)25℃时,将pH=9的NaOH溶液中C(OH-)=10-5 mol/L,pH=4的H2SO4溶液中C(H+)=10-4 mol/L,要使混合溶液呈中性,则氢氧根离子的物质的量等于氢离子的物质的量,设碱的体积为xL,酸的体积为yL,则10-5 mol/L×xL=10-4 mol/L×yL,
所以x:y=10-4:10-5=10:1,
故答案为:10:1;
(3)99℃时,pH1=a的某强酸溶液中C(H+)=10-a mol/L,pH2=b的某强碱溶液C(OH-)=10b-12 mol/L,溶液呈中性,则酸中氢离子的物质的量应等于碱中氢氧根离子的物质的量,所以100×10-a=1×10b-12,a+b=14,即pH1+pH2=14,故答案为:pH1+pH2=14;
(4)曲线B对应温度下,pH=2的盐酸溶液和pH=10的某BOH溶液等体积混合后,氢离子和氢氧根离子恰好反应,如果碱是强碱,则盐溶液呈中性,实际上溶液呈碱性,则碱为弱碱,生成强酸弱碱盐水解呈碱性,中和后混合溶液中还剩余较多的弱碱分子,可继续电离出OH-,使溶液呈碱性,
故答案为:BOH为弱碱,c(BOH)?c(HCl),等体积混合两溶液时,BOH过量,反应后溶液呈碱性.
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重考查分析计算能力,明确酸碱溶液混合时酸碱的物质的量关系及混合溶液pH的计算方法是解本题关键,题目难度中等.

| A. | 滴定管、移液管以及滴定过程中用于盛待测液的锥形瓶,使用前都需要洗涤与润洗 | |
| B. | 实验室制取氯气时,先装好二氧化锰,再检查装置的气密性 | |
| C. | 检验红色砖块中是否含三价铁的步骤为:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液 | |
| D. | 在中和热测定的实验中,将氢氧化钠溶液和盐酸混合反应后的最高温度作为末温度 |
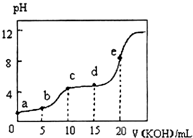 常温下,用0.10mol•L-1KOH溶液滴定10.00mL 0.10mol•L-1某二元弱酸H2R溶液,所得滴定曲线如图所示.下列叙述正确的是( )
常温下,用0.10mol•L-1KOH溶液滴定10.00mL 0.10mol•L-1某二元弱酸H2R溶液,所得滴定曲线如图所示.下列叙述正确的是( )| A. | a点所示溶液中:$\frac{c({H}^{+})}{c(O{H}^{-})}$<1012 | |
| B. | c点所示溶液中:c(K+)>c(HR-)>c(H2R)>c(R2-) | |
| C. | e点所示溶液中:c(H+)=c(HR-)+2c(H2R)+c(OH-) | |
| D. | 五个点中d点时c(HR-)最大 |
| 物质 | H2SO3 | HSO3- | H2CO3 | HCO3- |
| PKa | 1.9 | 7.2 | 6.4 | 10.3 |
(2)向10mL 0.01mol/L的H2SO3溶液中,滴加0.0lmol/L KOH溶液V(mL).
①当V=10mL时,溶液中存在:c(K+)>c(HSO3-)>c(SO32-)>c(H2SO3),则c(H+)>c(OH-)(选填“<”、“>”、“=”).
②当V=a mL时,溶液中离子浓度有如下关系:c(K+)=2c(SO32-)+c(HSO3-),该溶液呈中性(选填“酸”、“中”、“碱”).当V=b mL时,溶液中离子浓度有如下关系:c(K+)=c(SO32-)+c(HSO3--)+c(H2SO3),该溶液呈酸性(选填“酸”、“中”、“碱”),则a>b(选填“<”、“>”、“=”).
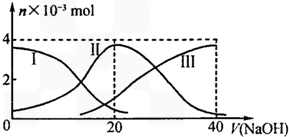 25℃时,向20mL0.2mol/LH2A溶液中滴加0.2mol/LNaOH溶液.有关微粒物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-).根据图示判断下列说法正确的是( )
25℃时,向20mL0.2mol/LH2A溶液中滴加0.2mol/LNaOH溶液.有关微粒物质的量变化如图(其中I代表H2A,II代表HA-,III代表A2-).根据图示判断下列说法正确的是( )| A. | 等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大 | |
| B. | 向Na2A溶液加入水的过程中,pH可能增大也可能减小 | |
| C. | 欲使NaHA溶液呈中性,可以向其中加入酸 | |
| D. | 当V(NaOH)=20mL时,溶液中离子浓度大小关系:[Na+]>[HA-]>[H+]>[A2-]>[OH-] |
| A. | 反应后盐水解使溶液呈碱性 | B. | 弱酸溶液和强碱溶液反应 | ||
| C. | 强酸溶液和弱碱溶液反应 | D. | 一元强酸溶液和一元强碱溶液反应 |
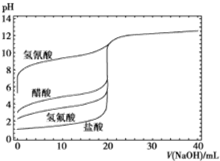 如图是用0.1mol/LNaOH溶液分别滴定20mL浓度均为0.1mol/L的不同一元酸的滴定曲线,下列说法错误的是( )
如图是用0.1mol/LNaOH溶液分别滴定20mL浓度均为0.1mol/L的不同一元酸的滴定曲线,下列说法错误的是( )| A. | 酸性:HF>CH3COOH>HCN | |
| B. | 用NaOH溶液滴定醋酸时,应用酚酞做指示剂不能使用甲基橙 | |
| C. | 当加入10mLNaOH溶液时,c(CN-)>c(CH3COO-) | |
| D. | 随NaOH溶液的滴入,CH3COOH溶液中水的电离程度先变大后变小 |
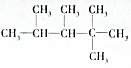 的烷烃,则此烯烃可能的结构简式是CH2=CHCH3CHCH3C(CH3)3、(CH3)2C=CCH3C(CH3)3、(CH3)2CHC=CH2C(CH3)3.
的烷烃,则此烯烃可能的结构简式是CH2=CHCH3CHCH3C(CH3)3、(CH3)2C=CCH3C(CH3)3、(CH3)2CHC=CH2C(CH3)3.