题目内容
某有机物燃烧后产物只有CO2和H2O,可推出的结论是这种有机物中( )
| A、一定只有C、H、O |
| B、可能含有C、H、O |
| C、一定含有C、H、无O |
| D、一定含有C、H、可能有O |
考点:测定有机物分子的元素组成
专题:烃及其衍生物的燃烧规律
分析:根据质量守恒定律,化学反应前后元素种类不变进行确定,有机物燃烧燃烧时一般有氧气参与,据此分析解答.
解答:
解:因有机物燃烧后产物只有CO2和H2O,从生成物中含有碳、氢元素,依据质量守恒定律可知该物质中一定含有碳、氢元素;
氧元素不能确定,可通过测定有机物及CO2和H2O的质量,若C、H两元素的质量之和等于有机物的质量,则该有机物只含C、H两元素;若C、H两元素的质量之和小于有机物的质量,则该有机物一定含有C、H、O三种元素,所以A、B、C错误,故D正确;
故选D.
氧元素不能确定,可通过测定有机物及CO2和H2O的质量,若C、H两元素的质量之和等于有机物的质量,则该有机物只含C、H两元素;若C、H两元素的质量之和小于有机物的质量,则该有机物一定含有C、H、O三种元素,所以A、B、C错误,故D正确;
故选D.
点评:本题考查有机物元素的确定,根据质量守恒定律,反应前后元素种类不变确定物质的组成是解题的关键,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
将4molA气体和2molB气体在2L的密闭容器中混合并在一定条件下发生如下反应:2A(g)+B(g)?2C(g)△H<0,4s后反应达到平衡状态,此时测得C的浓度为0.6mol?L-1,下列说法中正确的是( )
| A、当容器内混合气体的密度不再发生变化时,反应即达到平衡状态 |
| B、达平衡后若升高温度,该反应的平衡常数将增大 |
| C、平衡时反应物B的转化率为15.0% |
| D、达平衡后,如果此时移走2 molA和1molB,在相同温度下再达平衡时C的浓度<0.3mol?L-1 |
下列实验操作或记录的数据合理的是( )
| A、在中和反应反应热的测定实验中,用温度计轻轻搅拌混合液充分反应后再读数 |
| B、酸碱中和滴定前滴定管和锥形瓶先用滴定液润洗:2~3次 |
| C、配制硫酸亚铁溶液时,将FeSO4固体溶解在稀硫酸中并加人少量铁,再加水进行有关操作 |
| D、某学生用广泛pH试纸测得某稀盐酸的pH为2.3 |
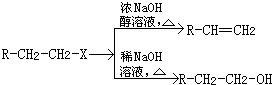
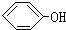 合成
合成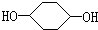 (部分试剂和反应条件已略去)
(部分试剂和反应条件已略去)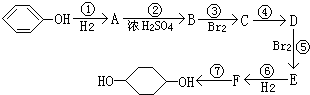
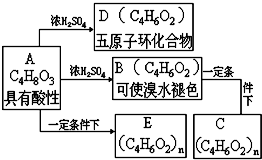 化合物C和E都是医用功能高分子材料,且组成中元素质量分数相同,均可由化合物A(C4H8O3)制得,如图所示.B和D互为同分异构体.
化合物C和E都是医用功能高分子材料,且组成中元素质量分数相同,均可由化合物A(C4H8O3)制得,如图所示.B和D互为同分异构体.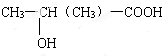 .
.
 几种常见物质之间存在如图转化关系,其中X、Y、Z为单质,其他物质均为化合 物.已知Y为无色无味气体,E为无色有刺激性气味气体,能使品红溶液退色,G溶液呈黄色,它们之间(部分产物及条件略去).请回答下列问题:
几种常见物质之间存在如图转化关系,其中X、Y、Z为单质,其他物质均为化合 物.已知Y为无色无味气体,E为无色有刺激性气味气体,能使品红溶液退色,G溶液呈黄色,它们之间(部分产物及条件略去).请回答下列问题: