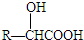题目内容
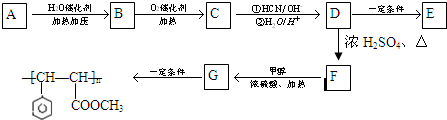
已知 (X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下:
(X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下:

回答下列问题:
(1)写出C中含氧官能团名称: ,F→G 的反应类型是 .
(2)写出A和新制Cu(OH)2悬浊液反应的化学方程式
(3)D的结构简式为 .
(4)F有多种同分异构体,写出同时满足下列条件的一种同分异构体的结构简式: .Ⅰ.分子中除苯环外,无其它环状结构Ⅱ.苯环上有两个处于对位的取代基III.能发生水解反应,不能与Na反应Ⅳ.能与新制Cu(OH)2按物质的量比1:2反应
(5)已知: (R,R′为烃基),试写出以苯和丙烯(CH2═CH-CH3)为原料,合成
(R,R′为烃基),试写出以苯和丙烯(CH2═CH-CH3)为原料,合成  的路线流程图(无机试剂任选).合成路线流程图示例如下:H2C═CH2
的路线流程图(无机试剂任选).合成路线流程图示例如下:H2C═CH2
CH3CH2Br
CH3CH2OH. .
 (X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下:
(X为卤原子,M为烃基或含酯基的取代基等),由有机物A合成G(香豆素)的步骤如下:
回答下列问题:
(1)写出C中含氧官能团名称:
(2)写出A和新制Cu(OH)2悬浊液反应的化学方程式
(3)D的结构简式为
(4)F有多种同分异构体,写出同时满足下列条件的一种同分异构体的结构简式:
(5)已知:
 (R,R′为烃基),试写出以苯和丙烯(CH2═CH-CH3)为原料,合成
(R,R′为烃基),试写出以苯和丙烯(CH2═CH-CH3)为原料,合成  的路线流程图(无机试剂任选).合成路线流程图示例如下:H2C═CH2
的路线流程图(无机试剂任选).合成路线流程图示例如下:H2C═CH2| HBr |
| NaOH溶液 |
| △ |
考点:有机物的合成
专题:有机物的化学性质及推断
分析:由有机物A合成G(香豆素)的路线可知,A能与新制氢氧化铜反应,则A为CH2=CHCHO,B为CH2=CHCOOH,B与甲醇发生酯化反应生成C,则C的结构简式为:CH2=CHCOOCH3,结合已知信息可知C+D→E,由E的结构可知,D为 ,E→F发生水解,F→G发生酯化反应,
,E→F发生水解,F→G发生酯化反应,
(1)C中含C=C和-COOC-,F→G发生酯化反应;
(2)A中含有醛基,能够与新制氢氧化铜发生反应生成CH2=CHCOONa、Cu2O和水;
(3)由上述分析可知,D为 ;
;
(4)F的同分异构体满足Ⅰ.分子中除苯环外,无其他环状结构;Ⅱ.苯环上有两个处于对位的取代基;Ⅲ.能发生水解反应,不能与金属Na反应;Ⅳ.能与新制的Cu(OH)2按物质的量之比1:2发生反应,则含-COOC-、-CHO或HCOOC-、-C-O-C-CH=CH2或HCOOC-、-COCH3;
(5)以苯、丙烯(CH2═CHCH3)为原料制备 ,先发生苯的取代,再结合信息可知,发生氯苯与的CH2═CHCH3反应,然后与水发生加成,最后与CO、Pb反应生成产物.
,先发生苯的取代,再结合信息可知,发生氯苯与的CH2═CHCH3反应,然后与水发生加成,最后与CO、Pb反应生成产物.
 ,E→F发生水解,F→G发生酯化反应,
,E→F发生水解,F→G发生酯化反应,(1)C中含C=C和-COOC-,F→G发生酯化反应;
(2)A中含有醛基,能够与新制氢氧化铜发生反应生成CH2=CHCOONa、Cu2O和水;
(3)由上述分析可知,D为
 ;
;(4)F的同分异构体满足Ⅰ.分子中除苯环外,无其他环状结构;Ⅱ.苯环上有两个处于对位的取代基;Ⅲ.能发生水解反应,不能与金属Na反应;Ⅳ.能与新制的Cu(OH)2按物质的量之比1:2发生反应,则含-COOC-、-CHO或HCOOC-、-C-O-C-CH=CH2或HCOOC-、-COCH3;
(5)以苯、丙烯(CH2═CHCH3)为原料制备
 ,先发生苯的取代,再结合信息可知,发生氯苯与的CH2═CHCH3反应,然后与水发生加成,最后与CO、Pb反应生成产物.
,先发生苯的取代,再结合信息可知,发生氯苯与的CH2═CHCH3反应,然后与水发生加成,最后与CO、Pb反应生成产物.解答:
解:由有机物A合成G(香豆素)的路线可知,A能与新制氢氧化铜反应,则A为CH2=CHCHO,B为CH2=CHCOOH,B与甲醇发生酯化反应生成C,则C的结构简式为:CH2=CHCOOCH3,结合已知信息可知C+D→E,由E的结构可知,D为 ,E→F发生水解,F→G发生酯化反应,
,E→F发生水解,F→G发生酯化反应,
(1)C中含C=C和-COOC-,含氧官能团为酯基,F→G发生酯化反应(取代反应),
故答案为:酯基;酯化反应(取代反应);
(2)A与新制氢氧化铜的反应方程式为:CH2=CHCHO+2Cu(OH)2+NaOH
CH2=CHCOONa+Cu2O↓+3H2O,
故答案为:CH2=CHCHO+2Cu(OH)2+NaOH
CH2=CHCOONa+Cu2O↓+3H2O;
(3)根据上述分析可知,D的结构简式为 ,故答案为:
,故答案为: ;
;
(4)F的同分异构体满足Ⅰ.分子中除苯环外,无其他环状结构;Ⅱ.苯环上有两个处于对位的取代基;Ⅲ.能发生水解反应,不能与金属Na反应;Ⅳ.能与新制的Cu(OH)2按物质的量之比1:2发生反应,则含-COOC-、-CHO或HCOOC-、-C-O-C-CH=CH2或HCOOC-、-COCH3,符合条件的同分异构体为 ,
,
故答案为: ;
;
(5)以苯、丙烯(CH2═CHCH3)为原料制备 ,先发生苯的取代,再结合信息可知,发生氯苯与的CH2═CHCH3反应,然后与水发生加成,最后与CO、Pb反应生成产物,合成路线流程图为
,先发生苯的取代,再结合信息可知,发生氯苯与的CH2═CHCH3反应,然后与水发生加成,最后与CO、Pb反应生成产物,合成路线流程图为 ,
,
故答案为: .
.
 ,E→F发生水解,F→G发生酯化反应,
,E→F发生水解,F→G发生酯化反应,(1)C中含C=C和-COOC-,含氧官能团为酯基,F→G发生酯化反应(取代反应),
故答案为:酯基;酯化反应(取代反应);
(2)A与新制氢氧化铜的反应方程式为:CH2=CHCHO+2Cu(OH)2+NaOH
| △ |
故答案为:CH2=CHCHO+2Cu(OH)2+NaOH
| △ |
(3)根据上述分析可知,D的结构简式为
 ,故答案为:
,故答案为: ;
;(4)F的同分异构体满足Ⅰ.分子中除苯环外,无其他环状结构;Ⅱ.苯环上有两个处于对位的取代基;Ⅲ.能发生水解反应,不能与金属Na反应;Ⅳ.能与新制的Cu(OH)2按物质的量之比1:2发生反应,则含-COOC-、-CHO或HCOOC-、-C-O-C-CH=CH2或HCOOC-、-COCH3,符合条件的同分异构体为
 ,
,故答案为:
 ;
;(5)以苯、丙烯(CH2═CHCH3)为原料制备
 ,先发生苯的取代,再结合信息可知,发生氯苯与的CH2═CHCH3反应,然后与水发生加成,最后与CO、Pb反应生成产物,合成路线流程图为
,先发生苯的取代,再结合信息可知,发生氯苯与的CH2═CHCH3反应,然后与水发生加成,最后与CO、Pb反应生成产物,合成路线流程图为 ,
,故答案为:
 .
.
点评:本题考查有机合成,题目难度中等,利用信息及合成流程图推断出各物质是解答本题的关键,注意熟练掌握常见有机物官能团与性质的关系,同分异构体的书写为难点,注意明确同分异构体的概念及书写原则.

练习册系列答案
相关题目
下列变化需要加入氧化剂才能实现的是( )
| A、HCl→H2 |
| B、NaCl→Cl2 |
| C、CuSO4→Cu |
| D、Na2CO3→CO2 |
下列各反应的离子方程式中,有错误的是( )
| A、氢氧化铝与盐酸反应:Al(OH)3+3H+═Al3++3H2O |
| B、氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-═BaSO4↓ |
| C、氯化亚铁溶液中滴入氯水:2Fe2++Cl2═2Fe3++2Cl- |
| D、氢氧化铝溶于氢氧化钠溶液:Al(OH)3+OH-═AlO2-+2H2O |
 常温下,用 0.1000mol?L-1NaOH溶液滴定 20.00mL 0.1000mol?L-1CH3COOH溶液所得滴定曲线如图.下列说法不正确的是( )
常温下,用 0.1000mol?L-1NaOH溶液滴定 20.00mL 0.1000mol?L-1CH3COOH溶液所得滴定曲线如图.下列说法不正确的是( )| A、点①所示溶液中:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| B、点②所示溶液中:c(Na+)=c(CH3COO-) |
| C、点③所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) |
| D、滴定过程中可能出现:c(CH3COOH)>c(H+)>c(CH3COO-)>c(Na+)>c(OH-) |