题目内容
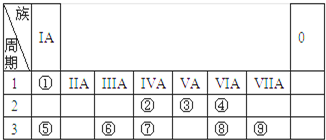
如表为元素周期表的一部分,请参照元素①~⑨在表中的位置,用化学用语回答下列问题:
(1)画出⑦的原子结构示意图 .
(2)②⑤⑥的原子半径由大到小的顺序为 (填元素符号);⑦⑧⑨的最高价含氧酸的酸性由强到弱的顺序是 (填化学式).
(3)②的单质与③、⑧的最高价氧化物对应水化物的浓溶液都能发生反应,其反应的化学方程式依次为 ; .
(4)X、Y是中学化学中的常见物质,X、Y分别由元素④、⑤和②、④形成,X与Y的反应是潜水艇和呼吸面具中氧气的来源.X中含有的化学键类型是 和 ;Y的电子式是 ;写出X、Y之间反应的化学方程式 ;当反应中有3.01×1023个电子转移时,参加反应的Y的质量是 g.

(1)画出⑦的原子结构示意图
(2)②⑤⑥的原子半径由大到小的顺序为
(3)②的单质与③、⑧的最高价氧化物对应水化物的浓溶液都能发生反应,其反应的化学方程式依次为
(4)X、Y是中学化学中的常见物质,X、Y分别由元素④、⑤和②、④形成,X与Y的反应是潜水艇和呼吸面具中氧气的来源.X中含有的化学键类型是
考点:位置结构性质的相互关系应用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:根据元素在周期表位置可知,①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是S,⑨是Cl,
(1)Si的质子数为14,核外有3个电子层,最外层电子数为4;
(2)电子层越多,半价越大,同周期原子序数大的半价小;非金属性越强,最高价含氧酸的酸性越强;
(3)C与浓硝酸反应生成二氧化碳、二氧化氮和水,C与浓硫酸反应生成二氧化硫、二氧化碳、水;
(4)X为Na2O2,Y为CO2,二者反应生成碳酸钠和氧气,2molNa2O2反应转移2mol电子,以此计算.
(1)Si的质子数为14,核外有3个电子层,最外层电子数为4;
(2)电子层越多,半价越大,同周期原子序数大的半价小;非金属性越强,最高价含氧酸的酸性越强;
(3)C与浓硝酸反应生成二氧化碳、二氧化氮和水,C与浓硫酸反应生成二氧化硫、二氧化碳、水;
(4)X为Na2O2,Y为CO2,二者反应生成碳酸钠和氧气,2molNa2O2反应转移2mol电子,以此计算.
解答:
解:根据元素在周期表位置可知,①是H,②是C,③是N,④是O,⑤是Na,⑥是Al,⑦是Si,⑧是S,⑨是Cl,
(1)Si的质子数为14,核外有3个电子层,最外层电子数为4,原子结构示意图为 ,故答案为:
,故答案为: ;
;
(2)电子层越多,半价越大,同周期原子序数大的半价小,②⑤⑥的原子半径由大到小的顺序为Na>Al>C;非金属性Cl>S>Si,则⑦⑧⑨的最高价含氧酸的酸性由强到弱的顺序是HClO4>H2SO4>H2SiO3,故答案为:Na>Al>C;HClO4>H2SO4>H2SiO3;
(3)C与浓硝酸反应生成二氧化碳、二氧化氮和水,C与浓硫酸反应生成二氧化硫、二氧化碳、水,反应分别为C+4HNO3(浓)=CO2↑+4NO2↑+2H2O、C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,故答案为:C+4HNO3(浓)=CO2↑+4NO2↑+2H2O;C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O;
(4)X为Na2O2,含离子键和共价键,其电子式为 ,Y为CO2,二者反应生成碳酸钠和氧气,该反应为2Na2O2+2CO2=2Na2CO3+O2,2molNa2O2反应转移2mol电子,当反应中有3.01×1023个电子转移时,即0.5mol电子转移参加反应的二氧化碳为0.5mol,所以参加反应的Y的质量是0.5mol×44g/mol=22g,
,Y为CO2,二者反应生成碳酸钠和氧气,该反应为2Na2O2+2CO2=2Na2CO3+O2,2molNa2O2反应转移2mol电子,当反应中有3.01×1023个电子转移时,即0.5mol电子转移参加反应的二氧化碳为0.5mol,所以参加反应的Y的质量是0.5mol×44g/mol=22g,
故答案为:离子键;共价键; ;2Na2O2+2CO2=2Na2CO3+O2;22.
;2Na2O2+2CO2=2Na2CO3+O2;22.
(1)Si的质子数为14,核外有3个电子层,最外层电子数为4,原子结构示意图为
 ,故答案为:
,故答案为: ;
;(2)电子层越多,半价越大,同周期原子序数大的半价小,②⑤⑥的原子半径由大到小的顺序为Na>Al>C;非金属性Cl>S>Si,则⑦⑧⑨的最高价含氧酸的酸性由强到弱的顺序是HClO4>H2SO4>H2SiO3,故答案为:Na>Al>C;HClO4>H2SO4>H2SiO3;
(3)C与浓硝酸反应生成二氧化碳、二氧化氮和水,C与浓硫酸反应生成二氧化硫、二氧化碳、水,反应分别为C+4HNO3(浓)=CO2↑+4NO2↑+2H2O、C+2H2SO4(浓)
| ||
| ||
(4)X为Na2O2,含离子键和共价键,其电子式为
 ,Y为CO2,二者反应生成碳酸钠和氧气,该反应为2Na2O2+2CO2=2Na2CO3+O2,2molNa2O2反应转移2mol电子,当反应中有3.01×1023个电子转移时,即0.5mol电子转移参加反应的二氧化碳为0.5mol,所以参加反应的Y的质量是0.5mol×44g/mol=22g,
,Y为CO2,二者反应生成碳酸钠和氧气,该反应为2Na2O2+2CO2=2Na2CO3+O2,2molNa2O2反应转移2mol电子,当反应中有3.01×1023个电子转移时,即0.5mol电子转移参加反应的二氧化碳为0.5mol,所以参加反应的Y的质量是0.5mol×44g/mol=22g,故答案为:离子键;共价键;
 ;2Na2O2+2CO2=2Na2CO3+O2;22.
;2Na2O2+2CO2=2Na2CO3+O2;22.
点评:本题考查位置、结构、性质的应用,涉及元素周期表中元素的位置、非金属性比较、电子式、化学反应方程式及有关计算等,综合性较强,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法不正确的是( )
| A、利用植物油的加成反应可以制得人造黄油 |
| B、75%的酒精可使蛋白质变性从而起到消毒作用 |
| C、纤维素在人体内可水解成葡萄糖,供人体组织的营养需要 |
D、可用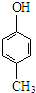 和HCHO为原料合成 和HCHO为原料合成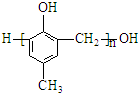 |

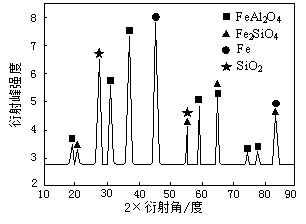
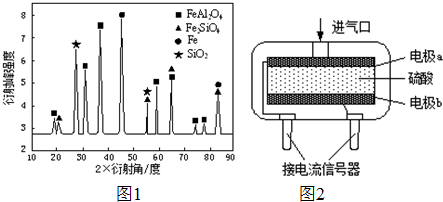

 短周期元素X、Y、Z、W在周期表中的位置如图1所示,其中W的氧化物是酸雨形成的主要物质.
短周期元素X、Y、Z、W在周期表中的位置如图1所示,其中W的氧化物是酸雨形成的主要物质.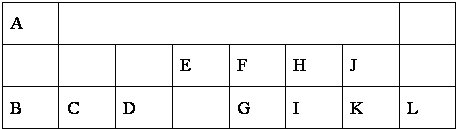
 )具有高度对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点.下面是立方烷衍生物I的一种合成路线:
)具有高度对称性、高致密性、高张力能及高稳定性等特点,因此合成立方烷及其衍生物成为化学界关注的热点.下面是立方烷衍生物I的一种合成路线: