题目内容
乙醇是重要的有机化工原料,可由乙烯气相直接水合法或间接水合法生产,回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),再水解生成乙醇,写出相应反应的化学方程式 ;
(2)已知:
甲醇脱水反应 2CH3OH(g)═CH3OCH3(g)+H2O(g)△H1=-23.9kJ?mol-1
甲醇制烯烃反应 2CH3OH(g)═C2H4(g)+2H2O(g)△H2=-29.1kJ?mol-1
乙醇异构化反应 C2H5OH(g)═CH3OCH3(g)△H3=+50.7kJ?mol-1
则乙烯气相直接水合反应C2H4(g)+H2O(g)═C2H5OH(g)的△H= kJ?mol-1,与间接水合法相比,气相直接水合法的优点是 ;
(3)如图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中nH2O:nC2H4=1:1)

①列式计算乙烯水合制乙醇反应在图中A点的平衡常数Kp= (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数);
②图中压强(P1,P2,P3,P4)大小顺序为 ,理由是 ;
③气相直接水合法常采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290℃,压强6.9MPa,nH2O:nC2H4=0.6:1,乙烯的转化率为5%,若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有 、 .
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),再水解生成乙醇,写出相应反应的化学方程式
(2)已知:
甲醇脱水反应 2CH3OH(g)═CH3OCH3(g)+H2O(g)△H1=-23.9kJ?mol-1
甲醇制烯烃反应 2CH3OH(g)═C2H4(g)+2H2O(g)△H2=-29.1kJ?mol-1
乙醇异构化反应 C2H5OH(g)═CH3OCH3(g)△H3=+50.7kJ?mol-1
则乙烯气相直接水合反应C2H4(g)+H2O(g)═C2H5OH(g)的△H=
(3)如图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中nH2O:nC2H4=1:1)

①列式计算乙烯水合制乙醇反应在图中A点的平衡常数Kp=
②图中压强(P1,P2,P3,P4)大小顺序为
③气相直接水合法常采用的工艺条件为:磷酸/硅藻土为催化剂,反应温度290℃,压强6.9MPa,nH2O:nC2H4=0.6:1,乙烯的转化率为5%,若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以采取的措施有
考点:真题集萃,热化学方程式,化学平衡常数的含义,化学平衡的影响因素,转化率随温度、压强的变化曲线
专题:化学反应中的能量变化,化学平衡专题
分析:(1)乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),效仿乙酸乙酯水解,将水分成氢原子和羟基生成乙醇和硫酸;
(2)利用盖斯定律构造目标热化学方程式并求焓变,气相直接水合法原子利用率100%;
(3)①列出Kp表达式,利用三段法计算平衡分压带入表达式计算即可;
②在相同温度下由于乙烯转化率为p1<p2<p3<p4,由C2H4(g)+H2O(g)═C2H5OH(g)可知正反应为气体体积减小的反应,根据压强对平衡移动的影响分析;
③若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以改变物质的浓度.
(2)利用盖斯定律构造目标热化学方程式并求焓变,气相直接水合法原子利用率100%;
(3)①列出Kp表达式,利用三段法计算平衡分压带入表达式计算即可;
②在相同温度下由于乙烯转化率为p1<p2<p3<p4,由C2H4(g)+H2O(g)═C2H5OH(g)可知正反应为气体体积减小的反应,根据压强对平衡移动的影响分析;
③若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以改变物质的浓度.
解答:
解:(1)乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H),化学方程式为C2H4+H2SO4=C2H5OSO3H,硫酸氢乙酯水解生成乙醇和硫酸,化学方程式为C2H5OSO3H+H2O→C2H5OH+H2SO4,
故答案为:C2H4+H2SO4=C2H5OSO3H、C2H5OSO3H+H2O→C2H5OH+H2SO4;
(2)已知:甲醇脱水反应 ①2CH3OH(g)═CH3OCH3(g)+H2O(g)△H1=-23.9kJ?mol-1
甲醇制烯烃反应 ②2CH3OH(g)═C2H4(g)+2H2O(g)△H2=-29.1kJ?mol-1
乙醇异构化反应 ③C2H5OH(g)═CH3OCH3(g)△H3=+50.7kJ?mol-1,
根据盖斯定律①-②-③可得:C2H4(g)+H2O(g)═C2H5OH(g)△H=(-23.9+29.1-50.7)kJ/mol=-45.5kJ/mol;
乙烯直接水化法中反应物中所有原子全部都变成生成物,所以原子利用率100%,没有副产品,
故答案为:-45.5;无副产品,原子利用率100%;
(3)①C2H4(g)+H2O(g)═C2H5OH(g)
开始:1 1 0
转化:0.2 0.2 0.2
平衡:0.8 0.8 0.2
乙醇占
=
,乙烯和水各占
=
,则乙醇的分压为7.85MPa×
=0.87MPa,乙烯和水的分压为7.85MPa×
=3.49MPa,
所以Kp=
=
=0.07(MPa)-1,
故答案为:0.07(MPa)-1;
②在相同温度下由于乙烯转化率为p1<p2<p3<p4,由C2H4(g)+H2O(g)═C2H5OH(g)可知正反应为气体体积减小的反应,所以增大压强,平衡正向移动,乙烯的转化率提高,因此压强关系是p1<p2<p3<p4,
故答案为:p1<p2<p3<p4;反应分子数减少,相同温度下,压强升高乙烯转化率提高;
③若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以改变物质的浓度,如从平衡体系中将产物乙醇分离出来,或增大水蒸气的浓度,改变二者物质的量的比等,
故答案为:将产物乙醇液化移去;增加nH2O:nC2H4比.
故答案为:C2H4+H2SO4=C2H5OSO3H、C2H5OSO3H+H2O→C2H5OH+H2SO4;
(2)已知:甲醇脱水反应 ①2CH3OH(g)═CH3OCH3(g)+H2O(g)△H1=-23.9kJ?mol-1
甲醇制烯烃反应 ②2CH3OH(g)═C2H4(g)+2H2O(g)△H2=-29.1kJ?mol-1
乙醇异构化反应 ③C2H5OH(g)═CH3OCH3(g)△H3=+50.7kJ?mol-1,
根据盖斯定律①-②-③可得:C2H4(g)+H2O(g)═C2H5OH(g)△H=(-23.9+29.1-50.7)kJ/mol=-45.5kJ/mol;
乙烯直接水化法中反应物中所有原子全部都变成生成物,所以原子利用率100%,没有副产品,
故答案为:-45.5;无副产品,原子利用率100%;
(3)①C2H4(g)+H2O(g)═C2H5OH(g)
开始:1 1 0
转化:0.2 0.2 0.2
平衡:0.8 0.8 0.2
乙醇占
| 0.2 |
| 0.8+0.8+0.2 |
| 1 |
| 9 |
| 0.8 |
| 0.8+0.8+0.2 |
| 4 |
| 9 |
| 1 |
| 9 |
| 4 |
| 9 |
所以Kp=
| p(C2H5OH) |
| p(C2H4)?p(H2O) |
| 0.87MPa |
| 3.49MPa×3.49MPa |
故答案为:0.07(MPa)-1;
②在相同温度下由于乙烯转化率为p1<p2<p3<p4,由C2H4(g)+H2O(g)═C2H5OH(g)可知正反应为气体体积减小的反应,所以增大压强,平衡正向移动,乙烯的转化率提高,因此压强关系是p1<p2<p3<p4,
故答案为:p1<p2<p3<p4;反应分子数减少,相同温度下,压强升高乙烯转化率提高;
③若要进一步提高乙烯转化率,除了可以适当改变反应温度和压强外,还可以改变物质的浓度,如从平衡体系中将产物乙醇分离出来,或增大水蒸气的浓度,改变二者物质的量的比等,
故答案为:将产物乙醇液化移去;增加nH2O:nC2H4比.
点评:本题考查了化学方程式的书写、压强对平衡移动的影响、物质制取方案的比较、反应热及平衡常数的计算等知识,综合性非常强,该题是高考中的常见题型,属于中等难度较大,侧重于学生分析问题、解决问题、知识迁移能力的培养.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
芳香化合物M的结构简式为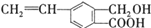 ,关于有机物M的说法正确的是( )
,关于有机物M的说法正确的是( )
 ,关于有机物M的说法正确的是( )
,关于有机物M的说法正确的是( )| A、有机物M的分子式为C10H12O3 |
| B、1mol Na2CO3最多能消耗1mol有机物M |
| C、1mol M和足量金属钠反应生成22.4L气体 |
| D、有机物M能发生取代、氧化和加成反应 |
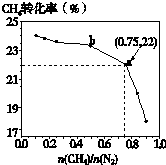 已知:3CH4(g)+2N2(g)
已知:3CH4(g)+2N2(g)| 700℃ |
| 催化剂 |
| n(CH4) |
| n(N2) |
A、
| ||
B、
| ||
| C、b点对应的平衡常数比a点的大 | ||
| D、a点对应的NH3的体积分数约为26% |