题目内容
8.下图关于各实验装置(夹持装置已略去)的叙述,正确的是( )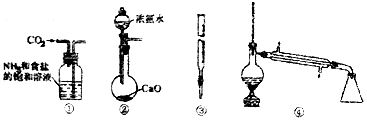
| A. | 装置①可用于模拟侯氏制碱法制取碳酸氢钠 | |
| B. | 装置②可用于制备少量NH3 | |
| C. | 装置③可用于准确取一定体积酸性KMnO4标准溶液 | |
| D. | 装置④常用于分离互不相溶的液体混合物 |
分析 A.气体应长导管进入;
B.浓氨水与CaO混合可制备氨气,为固液反应不加热原理;
C.图中为碱式滴定管,酸性KMnO4可氧化橡胶;
D.分离互不相溶的液体混合物,为分液法.
解答 解:A.气体应长导管进入,图中气体的进入方向不合理,故A错误;
B.浓氨水与CaO混合可制备氨气,为固液反应不加热原理,则图中装置可制备氨气,故B正确;
C.图中为碱式滴定管,酸性KMnO4可氧化橡胶,应选酸式滴定管,故C错误;
D.分离互不相溶的液体混合物,为分液法,选择分液漏斗,而图中为蒸馏装置,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,侧重分析与实验能力的考查,把握实验装置的作用、物质的制备实验、中和滴定、混合物分离提纯、实验技能为解答的关键,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
4.FeCl2是一种常用的还原剂.有关数据如下:
查阅资料知:氯化铁遇水剧烈水解.实验室可以用如下方法来制备无水FeCl2.
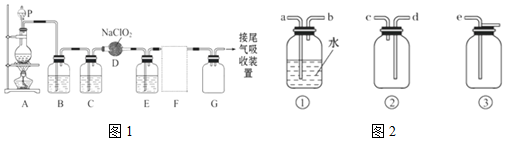
按图装置,在三颈烧瓶中放入a g无水氯化铁和过量的氯苯,控制反应温度在128~139℃加热3h,冷却,分离提纯得到粗产品.

回答下列问题:
(1)上述生成FeCl2的反应中,还原剂是C6H5Cl.
(2)实验装置中,仪器B的作用是防止安全瓶内的水分进入A装置,导致FeCl2变质,虚线框内应选择的安全瓶(盛有蒸馏水)是c.(填标号)
(3)实验过程中控制反应温度接近或超过C6H5Cl的沸点,C6H5Cl不会有明显损失,原因是_实验使用了冷凝回流装置.
(4)冷却反应后的实验装置,对三颈烧瓶内的物质进行过滤、洗涤、干燥,得到粗产品.
①洗涤沉淀所用的试剂应为b.(填标号)
a.蒸馏水 b.苯 c.烧碱溶液
②回收滤液中C6H5Cl的方案为蒸馏滤液,并收集132℃馏分.
(5)用x mol•L-1NaOH溶液滴定安全瓶中得到的盐酸,消耗少y mLNaOH溶液,则反应中氯化铁的转化率为$\frac{x•y×1{0}^{-3}×2×162.5}{a}×100%$(只列出计算式).
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38此温度下在实验室中配制100mL5.0mol•L-1,FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入2mol•L-1的盐酸2.5mL(总体积忽略加入盐酸体积).
| C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl、C6H4Cl2、苯,易吸水. | ||
| 熔点/℃ | -45 | 53 | -- | -- |
| 沸点/℃ | 132 | 173 | -- | -- |
按图装置,在三颈烧瓶中放入a g无水氯化铁和过量的氯苯,控制反应温度在128~139℃加热3h,冷却,分离提纯得到粗产品.

回答下列问题:
(1)上述生成FeCl2的反应中,还原剂是C6H5Cl.
(2)实验装置中,仪器B的作用是防止安全瓶内的水分进入A装置,导致FeCl2变质,虚线框内应选择的安全瓶(盛有蒸馏水)是c.(填标号)
(3)实验过程中控制反应温度接近或超过C6H5Cl的沸点,C6H5Cl不会有明显损失,原因是_实验使用了冷凝回流装置.
(4)冷却反应后的实验装置,对三颈烧瓶内的物质进行过滤、洗涤、干燥,得到粗产品.
①洗涤沉淀所用的试剂应为b.(填标号)
a.蒸馏水 b.苯 c.烧碱溶液
②回收滤液中C6H5Cl的方案为蒸馏滤液,并收集132℃馏分.
(5)用x mol•L-1NaOH溶液滴定安全瓶中得到的盐酸,消耗少y mLNaOH溶液,则反应中氯化铁的转化率为$\frac{x•y×1{0}^{-3}×2×162.5}{a}×100%$(只列出计算式).
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38此温度下在实验室中配制100mL5.0mol•L-1,FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入2mol•L-1的盐酸2.5mL(总体积忽略加入盐酸体积).
19.下列关于乙烯的说法错误的是( )
| A. | 乙烯的化学性质比乙烷活泼 | B. | 乙烯的比例模型可表示为  | ||
| C. | 可作香蕉等水果的催熟剂 | D. | 燃烧时火焰明亮,同时产生黑烟 |
16.以下实验操作及现象合理的是( )
| A. | 为检验SO42-需要滴加稀硝酸酸化的BaCl2溶液并观察是否有白色沉淀生成 | |
| B. | 把光洁无锈的铁丝放在煤气灯外焰灼烧至与原来的火焰颜色相同时,蘸取K2CO3溶液并灼烧,透过蓝色钴玻璃可观察到火焰为淡紫色 | |
| C. | 向盛有足量苯酚溶液的试管中滴加少量稀溴水,可观察到白色沉淀生成 | |
| D. | 实验室制备乙炔时,常用NaOH溶液除去产生的H2S、PH3等杂质 |
3.下列关于有机物的来源、结构与性质说法正确的是( )
| A. | 甲烷是正四面体结构,性质活泼,常温下能与强酸、强碱发生剧烈反应 | |
| B. | 乙烯是通过石油裂解得到的,属于不饱和烃 | |
| C. | 苯与氢气、液溴、浓硝酸的反应类型相同 | |
| D. | 乙酸又名醋酸,其官能团是醚基,可以与乙醇发生反应生成乙酸乙酯 |
13.下列关于元素性质说法正确的是( )
| A. | Li、C、P分别在氧气中燃烧均能生成两种相应的氧化物 | |
| B. | 除去CO2中混有的SO2气体可选用Na2SO3溶液或NaHCO3溶液 | |
| C. | 过量的铁粉与氯气在点燃条件下充分反应,生成氯化亚铁 | |
| D. | SiO2既可以与氢氟酸反应,又可以与氢氧化钠溶液反应,所以SiO2是两性氧化物 |
20.下列关于实验原理或操作的叙述中,不正确的是( )
| A. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| B. | 乙醇发生催化氧化反应,产物可用新制的Cu(OH)2悬浊液检验 | |
| C. | 加入浓CuSO4溶液能使蛋白质溶液发生盐析现象 | |
| D. | 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 |