题目内容
16.硫及其化合物在生产和生活中都发挥着重要的作用.(1)SO2是形成酸雨的主要污染物,燃煤脱硫的原理为2CaO(s)+2SO2(s)+O2(g)?2CaSO4(s)
向10L恒温恒容密闭容器中加入3mol CaO,并通入2mol SO2和lmol O2发生上述反应,2min时达平衡,此时CaSO4为l.8mol.0〜2min内,用SO2表示的该反应的速率v(SO2)=0.09mol/(L•min);其他条件保持不变,若上述反应在恒压条件下进行,达到平衡时SO2的转化率增大(“增大”、“减小”或“不变”).
(2)25℃时,H2SO3的电离常数Kal=1×10-2,Ka2=6×10-8,则该温度下NaHSO3的水解平衡常数Kb=1×10-12.判断NaHSO3溶液显酸性(填“酸”、“碱”或“中”),用简要文字叙述原因是HSO3-电离大于水解.
(3)Na2SO3溶液作为吸收液可脱除烟气中的SO2.当吸收液的pH降至约为6时,需送至电解槽再生.再生示意图如下:

HSO3-在阳极放电时的电极反应式是HSO3-+H2O-2e-=SO42-+3H+.
(4)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应
TaS2(s)+2I2(g)?TaI4(g)+S2(g)△H>0

如上图所示,上述反应在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2 (g),-段时间后,在溫度为T1的一端得到了纯净的TaS2晶体,则温度T1<T2 (填“>”“<”或“=”)上述反应体系中循环使用的物质是I2.
分析 (1)先根据反应方程式计算出平衡时消耗二氧化硫的物质的量,然后根据v=$\frac{\frac{△n}{V}}{△t}$计算出0~2min内用SO2(g)表示的该反应的速率;反应在恒压条件下进行,随反应进行,气体体积减小,为保持恒压所以容器体积减小,压强比恒容容器大,平衡正向进行,平衡时SO2的转化率增大;
(2)NaHSO3的水解平衡常数Kb=$\frac{c({H}_{2}S{O}_{3})×c(O{H}^{-})}{c(HS{{O}_{3}}^{-})}$=$\frac{Kw}{{K}_{a1}}$;根据Kb与Ka2的相对大小分析酸碱性;
(3)阳极上阴离子放电发生氧化反应;
(4)通过题意温度T2端利于反应正向进行,为高温,温度T1端利于反应向左进行,为低温,所以T1<T2.
解答 解:(1)2min时达平衡,此时CaSO4(s)为1.8mol,根据反应2CaO(s)+2SO2(g)+O2(g)?2CaO4(s)可知平衡时消耗二氧化硫的物质的量为:1.8mol×$\frac{2}{2}$=1.8mol,
则0~2min内,用SO2(g)表示的该反应的速率为:v(SO2)=$\frac{\frac{1.8mol}{10L}}{2min}$=0.09mol/(L•min);反应在恒压条件下进行,随反应进行,气体体积减小,为保持恒压所以容器体积减小,压强比恒容容器大,平衡正向进行,平衡时SO2的转化率增大,
故答案为:0.09mol/(L•min);增大;
(2)NaHSO3的水解平衡常数Kb=$\frac{c({H}_{2}S{O}_{3})×c(O{H}^{-})}{c(HS{{O}_{3}}^{-})}$=$\frac{Kw}{{K}_{a1}}$=$\frac{1.0×1{0}^{-14}}{1.0×1{0}^{-2}}$=1×10-12;NaHSO3的水解显碱性,NaHSO3电离显酸性,由于水解常数小于电离常数(Ka2),所以NaHSO3在溶液中以电离为主,即溶液显酸性;原因是HSO3-电离大于水解;
故答案为:1×10-12;酸性;HSO3-电离大于水解;
(3)当吸收液的pH降至约为6时,吸收液中阴离子主要是亚硫酸氢根离子,亚硫酸氢根离子在阳极上失电子和水反应生成硫酸根离子和氢离子,电极反应式为:HSO3-+H2O-2e-=SO42-+3H+.
故答案为:HSO3-+H2O-2e-=SO42-+3H+;
(4)由所给方程式可知该反应为吸热反应,通过题意温度T2端利于反应正向进行,为高温,温度T1端利于反应向左进行,为低温,所以T1<T2,I2是可以循环使用的物质;
故答案为:<;I2.
点评 本题考查转化率,化学反应速率,水解平衡常数,溶液酸碱性的判断,电极方程式的书写,平衡的移动等知识,难度较大.

| 选项 | 实验操作和现象 | 结论 |
| A | 将气体X分别通入溴水和酸性高锰酸钾溶液中,两溶液均褪色 | 气体X一定是C2H4 |
| B | 向NaAlO2溶液中滴入NaHCO3溶液,产生白色沉淀 | AlO2-结合H+的能力比CO32--强 |
| C | 向某溶液中先滴加少量氯水,再滴加2滴KSCN溶液,溶液变成血红色 | 原溶液中一定含有Fe2+ |
| D | 将H2S气体通入浓度均为0.01mol•L-l的ZnSO4和CuSO4混合溶液中,先出现CuS黑色沉淀 | Ksp(CuS)<Ksp(ZnS) |
| A. | A | B. | B | C. | C | D. | D |
| A. | c(N2)=2.25 mol/L | B. | c(NH3)=1.9 mol/L | C. | c(H2)=0.3 mol/L | D. | c(N2)=1.3mol/L |
| C6H5Cl(氯苯) | C6H4Cl2 | FeCl3 | FeCl2 | |
| 溶解性 | 不溶于水,易溶于苯 | 不溶于C6H5Cl、C6H4Cl2、苯,易吸水. | ||
| 熔点/℃ | -45 | 53 | -- | -- |
| 沸点/℃ | 132 | 173 | -- | -- |
按图装置,在三颈烧瓶中放入a g无水氯化铁和过量的氯苯,控制反应温度在128~139℃加热3h,冷却,分离提纯得到粗产品.

回答下列问题:
(1)上述生成FeCl2的反应中,还原剂是C6H5Cl.
(2)实验装置中,仪器B的作用是防止安全瓶内的水分进入A装置,导致FeCl2变质,虚线框内应选择的安全瓶(盛有蒸馏水)是c.(填标号)
(3)实验过程中控制反应温度接近或超过C6H5Cl的沸点,C6H5Cl不会有明显损失,原因是_实验使用了冷凝回流装置.
(4)冷却反应后的实验装置,对三颈烧瓶内的物质进行过滤、洗涤、干燥,得到粗产品.
①洗涤沉淀所用的试剂应为b.(填标号)
a.蒸馏水 b.苯 c.烧碱溶液
②回收滤液中C6H5Cl的方案为蒸馏滤液,并收集132℃馏分.
(5)用x mol•L-1NaOH溶液滴定安全瓶中得到的盐酸,消耗少y mLNaOH溶液,则反应中氯化铁的转化率为$\frac{x•y×1{0}^{-3}×2×162.5}{a}×100%$(只列出计算式).
(6)已知25℃时,Ksp[Fe(OH)3]=4.0×10-38此温度下在实验室中配制100mL5.0mol•L-1,FeCl3溶液,为使配制过程中不出现浑浊现象,则至少需要加入2mol•L-1的盐酸2.5mL(总体积忽略加入盐酸体积).
| A. | 常温下1molCl2和足量氢氧化钠溶液充分反应,转移电子数目为2NA | |
| B. | 12 g石墨烯(单层石墨)中含有六元环的个数为0.5NA | |
| C. | 0.1molFe与稀硝酸恰好反应完后,溶液中NO3-的数目为0.3NA | |
| D. | l L pH=l的硫酸溶液中含有的H+数为0.2NA |
| A. | 苯中加入溴水后溴水层颜色变浅,这是由于发生了取代反应 | |
| B. | 乙烯和苯分子中所有原子在同一平面上 | |
| C. | 一氯丙烷(C3H7Cl)的同分异构体共有3种 | |
| D. | 标准状况下,2.24LCHCl3含有的分子数为0.1NA |
| A. | 乙烯的化学性质比乙烷活泼 | B. | 乙烯的比例模型可表示为  | ||
| C. | 可作香蕉等水果的催熟剂 | D. | 燃烧时火焰明亮,同时产生黑烟 |
| A. | 从碘水中提取单质碘时,不能用无水乙醇代替CCl4 | |
| B. | 乙醇发生催化氧化反应,产物可用新制的Cu(OH)2悬浊液检验 | |
| C. | 加入浓CuSO4溶液能使蛋白质溶液发生盐析现象 | |
| D. | 实验室中提纯混有少量乙酸的乙醇,可采用先加生石灰,过滤后再蒸馏的方法 |
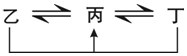 有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、并能使红色湿润石蕊试纸变蓝,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.下图中均含D或F元素的物质均会有图示转化关系:
有A、B、C、D、E、F六种前四周期的元素,原子序数依次增大,A、B、C、D、E均为短周期元素,D和F元素对应的单质为日常生活中常见金属.A原子核内只有一个质子,元素A与B形成的气态化合物甲具有10e-、并能使红色湿润石蕊试纸变蓝,C元素原子的最外层电子数是其电子层数的3倍,C与E同主族.下图中均含D或F元素的物质均会有图示转化关系: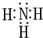 .
.