题目内容
16.下列事实能说明醋酸是弱电解质的是( )①醋酸与水以任意比例互溶
②醋酸溶液能导电
③醋酸溶液中存在醋酸分子④测得醋酸的pH比盐酸pH大
⑤在漂白剂溶液中滴加醋酸能增强漂白效果
⑥0.1mol/L醋酸溶液的pH=2
⑦CH3COOK溶液能使酚酞试液变红色
⑧大小相同的锌粒与相同物质的量浓度的盐酸和醋酸反应,醋酸产生氢气速率慢.
| A. | ①④⑥⑧ | B. | ②④⑥⑦ | C. | ④⑤⑥⑧ | D. | ③⑥⑦⑧ |
分析 弱电解质在溶液中不完全电离的电解质,可以根据醋酸的电离程度及醋酸钠溶液的酸碱性判断醋酸的强弱.
解答 解:①醋酸与水以任意比例互溶,说明醋酸的溶解度大,而不能证明醋酸的电离程度,所以不能证明醋酸为弱酸,故错误;
②醋酸溶液能导电,说明醋酸在水溶液里能电离出阴阳离子,为电解质,而不能证明醋酸的电离程度,所以不能证明醋酸为弱酸,故错误;
③醋酸溶液中存在醋酸分子,说明醋酸部分电离,即能证明醋酸为弱电解质,故正确;
④测得醋酸的pH比盐酸pH大,但是不知道二者的浓度,所以不能确定醋酸是否完全电离,则不能证明醋酸为弱酸,故错误;
⑤在漂白剂溶液中滴加醋酸能增强漂白效果,说明醋酸能电离出氢离子,但是不能确定醋酸是否完全电离,则不能证明醋酸为弱酸,故错误;
⑥0.1mol/L醋酸溶液的pH=2,说明醋酸部分电离,即能证明醋酸为弱电解质,故正确;
⑦CH3COOK溶液能使酚酞试液变红色,说明醋酸根离子发生水解溶液显碱性,即醋酸为弱酸,即能证明醋酸为弱电解质,故正确;
⑧大小相同的锌粒与相同物质的量浓度的盐酸和醋酸反应,醋酸产生氢气速率慢,说明醋酸中氢离子浓度小,即醋酸不完全电离,能证明醋酸为弱电解质,故正确;
故选D.
点评 本题考查了强弱电解质的判断,根据电解质的电离程度确定电解质的强弱,可以从醋酸溶液中醋酸浓度与pH的相对大小、醋酸钠溶液的酸碱性来确定,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.美好的生活离不开化学,我们应感恩化学,掌握必要的化学知识.下列说法错误的是( )
| A. | 合理使用化肥可以提高农作物的产量 | |
| B. | 二氧化氯、臭氧均可用作自来水消毒剂 | |
| C. | 氢氧化铝和碳酸钠均可用于治疗胃酸过多 | |
| D. | 化妆品中的甘油可起到保湿滋润皮肤的作用 |
1.下列说法中正确的是( )
| A. | 100mL pH=3的盐酸和醋酸溶液,与足量锌反应,起始时二者产生氢气的速率基本相等 | |
| B. | 100mL 1mol/L的盐酸和50mL 2mol/L的盐酸分别与足量的锌反应,二者放出氢气的速率和质量均相等 | |
| C. | 100mL pH=3的盐酸和醋酸溶液,与足量锌反应后,所得氢气的质量相等 | |
| D. | 100mL 0.1mol/L的硫酸和盐酸溶液,与足量锌反应后,前者放出氢气的质量与后者相等 |
8.常温时,将VlmL c1mol/L的醋酸溶液滴加到V2mL c2mol/L 的烧碱溶液中,下列结论正确的是( )
| A. | 若Vl=V2,且混合溶液pH<7,则必有c1<c2 | |
| B. | 若混合溶液的pH=7,则混合溶液中c(Na+)=c (CH3COO-)+c(CH3COOH ) | |
| C. | 若混合溶液的pH>7,则混合溶液中c(Na+)<c( CH3COO-) | |
| D. | 若Vl=V2,c1=c2,则混合溶液中c(OH-)=c(CH3COOH)+c(H+) |
6.现有常温下pH=2的盐酸甲和pH=2的CH3COOH溶液乙,请根据下列操作回答问题:
(1)取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),醋酸的电离平衡向左(填“向左”、“向右”或“不”)移动;常温下,另取10mL的乙溶液,加水稀释过程中,下列表达式的数据一定增大的是BD.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)< V(乙)( 填“>”、“<”或“=”).
(3)已知25℃时,两种酸的电离平衡常数如下:
下列四种离子水解程度最大的是B.
A.HCO3- B.CO32- C.ClO- D.CH3COO-
(4)常温下,取99mL甲溶液与1mL1mol/L的NaOH溶液混合(忽略溶液体积变化),恢复至常温时其pH=10.
(1)取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),醋酸的电离平衡向左(填“向左”、“向右”或“不”)移动;常温下,另取10mL的乙溶液,加水稀释过程中,下列表达式的数据一定增大的是BD.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(2)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)< V(乙)( 填“>”、“<”或“=”).
(3)已知25℃时,两种酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K1 | 1.8×10-5 | 4.3×10-7 | 3.0×10-8 |
| K2 | -- | 5.6×10-11 | -- |
A.HCO3- B.CO32- C.ClO- D.CH3COO-
(4)常温下,取99mL甲溶液与1mL1mol/L的NaOH溶液混合(忽略溶液体积变化),恢复至常温时其pH=10.




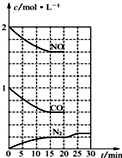 研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.