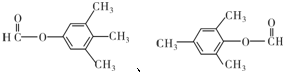题目内容
4.设NA为阿伏加德罗常数的值.下列说法一定正确的是( )| A. | 100 mL 1 mol/L的盐酸中含HCl分子数为0.1NA | |
| B. | 7.8 g Na2O2和Na2S的混合物中阴离子数目为0.2NA | |
| C. | 标准状况下,2.24 L SO3中含有氧原子数目为0.3NA | |
| D. | 2 g D216O中含中子、质子、电子数目均为NA |
分析 A、HCl溶于水后能完全电离;
B、Na2O2和Na2S的摩尔质量均为78g/mol,且均由2个钠离子和1个阴离子构成;
C、标况下三氧化硫为固体;
D、求出2 g D216O的物质的量,然后根据重水中含10个电子、10个质子和10个中子来分析.
解答 解:A、HCl溶于水后能完全电离,故盐酸溶液中无氯化氢分子,故A错误;
B、Na2O2和Na2S的摩尔质量均为78g/mol,故7.8g混合物的物质的量为0.1mol,且两者均由2个钠离子和1个阴离子构成,故0.1mol混合物中含0.1NA个阴离子,故B错误;
C、标况下三氧化硫为固体,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、2 g D216O的物质的量为0.1mol,而重水中含10个电子、10个质子和10个中子,故0.1mol重水中含电子、质子和中子个数均为NA个,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.元素A、B、C、D分别位于三个不同短周期,且原子序数依次增大.只有D为金属元素,它们可形成x、y、z、w四种常见的二元化合物及p、q两种常见三元化合物,它们之间存在如下转化关系;①x$\stackrel{z}{→}$p$\stackrel{w}{→}$q+z,②y$\stackrel{z}{→}$p+O2↑,其中z为液体、w为气体,其余均为固体.下列有关说法正确的是( )
| A. | 原子半径大小顺序:D>C>B>A | |
| B. | y、p 中均只含有离子键 | |
| C. | B、D两元素最高价氧化物对应水化物分别为强酸、强碱 | |
| D. | p能抑制水的电离而q能促进水的电离 |
19.蜂蜜是家庭生活中常见的一种营养品.下表是某品牌蜂蜜外包装上标识的“营养成分表”
说明:表中所列“碳水化合物”主要指一些糖类物质.
(1)在六大基本营养素中,除水之外,上表中没有列出的是维生素;
(2)表中的“钠”是指钠元素,
(3)服用蜂蜜可有效补充人体所需能量,其中提供能量的主要是碳水化合物(或糖类).
(4)麦芽糖(C12H22O11)是蜂蜜中的一种碳水化合物,它在一定条件下可实现如下转化:C12H22O11+X═2C6H12O6,X的化学式为H2O,反应类型是化合反应.
| 项 目 | 每100克(g) | 营养素参考值% |
| 能 量 | 1500kJ | 18% |
| 蛋 白 质 | 0g | 0% |
| 脂 肪 | 2.0g | 3% |
| 碳水化合物 | 72g | 24% |
| 钠 | 30mg | 2% |
(1)在六大基本营养素中,除水之外,上表中没有列出的是维生素;
(2)表中的“钠”是指钠元素,
(3)服用蜂蜜可有效补充人体所需能量,其中提供能量的主要是碳水化合物(或糖类).
(4)麦芽糖(C12H22O11)是蜂蜜中的一种碳水化合物,它在一定条件下可实现如下转化:C12H22O11+X═2C6H12O6,X的化学式为H2O,反应类型是化合反应.
2.相同温度下,将足量的AgCl分别放入下列溶液中:①40mL 0.02mol/L BaCl2溶液②40mL 0.03mol/L 盐酸 ③10mL 蒸馏水 ④50mL0.05mol/L AgNO3溶液,则AgCl的溶解度大小顺序为( )
| A. | ①=②=③=④ | B. | ③>②>①>④ | C. | ④>②>①>③ | D. | ③>①>②>④ |
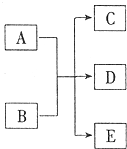 一定条件,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.
一定条件,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.
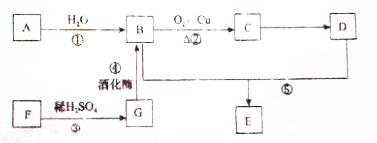
 探究上述四种酸的氧化性相对强弱及其与铜反应的还原产物的性质:
探究上述四种酸的氧化性相对强弱及其与铜反应的还原产物的性质:
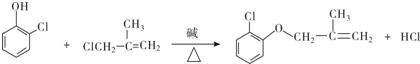 (有机物用结构简式表示,下同).
(有机物用结构简式表示,下同).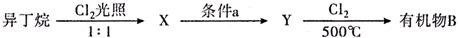
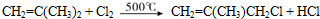 ;
;