题目内容
15.元素A、B、C、D分别位于三个不同短周期,且原子序数依次增大.只有D为金属元素,它们可形成x、y、z、w四种常见的二元化合物及p、q两种常见三元化合物,它们之间存在如下转化关系;①x$\stackrel{z}{→}$p$\stackrel{w}{→}$q+z,②y$\stackrel{z}{→}$p+O2↑,其中z为液体、w为气体,其余均为固体.下列有关说法正确的是( )| A. | 原子半径大小顺序:D>C>B>A | |
| B. | y、p 中均只含有离子键 | |
| C. | B、D两元素最高价氧化物对应水化物分别为强酸、强碱 | |
| D. | p能抑制水的电离而q能促进水的电离 |
分析 四种元素分别位于三个不同短周期且A的原子序数最小,则A为H元素,由两种短周期元素形成的二元化合物发生反应有氧气生成和z为常见液体可知z为H2O,y为Na2O2,根据反应①可知x为Na2O,p为NaOH,w为CO2或SO2,q为Na2CO3或Na2SO3,结合原子序数关系及D为金属可知B为C元素,C为O元素,D为Na元素,则w为CO2,q为Na2CO3,结合对应物质的性质以及元素周期率知识解答该题.
解答 解:四种元素分别位于三个不同短周期且A的原子序数最小,则A为H元素,由两种短周期元素形成的二元化合物发生反应有氧气生成和z为常见液体可知z为H2O,y为Na2O2,根据反应①可知x为Na2O,p为NaOH,w为CO2或SO2,q为Na2CO3或Na2SO3,结合原子序数关系及D为金属可知B为C元素,C为O元素,D为Na元素,则w为CO2,q为Na2CO3,
A.B为C元素,C为O元素,同周期元素从左到右原子半径逐渐减小,原子半径B>C,故A错误;
B.y为Na2O2,p为NaOH,含有离子键和共价键,故B错误;
C.知B为C元素,对应的最高价氧化物的水化物为碳酸,属于弱酸,故C错误;
D.q为Na2CO3,水解呈碱性,促进水的电离,加入氢氧化钠可抑制碳酸钠的水解,故D正确.
故选D.
点评 本题考查无机物的推断,为高频考点和常见题型,侧重于学生的分析能力的考查,注意把握物质的性质以及元素在周期表的中位置和元素周期率知识,难度不大,本题解答的关键是水的状态、过氧化钠和水的反应,难度中等.

练习册系列答案
相关题目
5.苹果酸的结构简式如图所示,下列说法正确的是( )
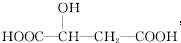
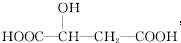
| A. | 苹果酸中能发生酯化反应的官能团有1种 | |
| B. | 1 mol苹果酸可与3 mol NaHCO3发生中和反应 | |
| C. | 1 mol苹果酸与足量金属 Na反应生成生成mol H2 | |
| D. | 1 mol苹果酸可以形成三元或四元环状内酯 |
6.下列说法不正确的是( )
| A. | 金刚石跟石墨是同素异形体 | B. | 126C和146C是同位素 | ||
| C. | 不同的核素质子数可能相同 | D. | C2H4和C3H6一定是同系物 |
3.下列说法正确的是( )
| A. | 乙醇和乙二醇互为同系物 | |
| B. | 异丙苯(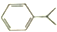 )分子中碳原子可能都处于同一平面 )分子中碳原子可能都处于同一平面 | |
| C. | 按系统命名法,化合物(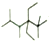 )的名称是2,3,5,5一四甲基一4,4一二乙基己烷 )的名称是2,3,5,5一四甲基一4,4一二乙基己烷 | |
| D. | 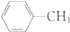 的一溴代物和 的一溴代物和 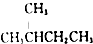 的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) |
20.阿伏加德罗常数是物理学和化学中的一个重要常量.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 在常温常压下,11.2L Cl2含有的分子数为0.5NA | |
| B. | 在常温常压下,25.5g NH3所含的原子数为6NA | |
| C. | 标准状况下,11.2L水所含的分子数为0.5NA | |
| D. | 在同温同压下,相同体积的任何气体单质所含的原子数相同 |
4.设NA为阿伏加德罗常数的值.下列说法一定正确的是( )
| A. | 100 mL 1 mol/L的盐酸中含HCl分子数为0.1NA | |
| B. | 7.8 g Na2O2和Na2S的混合物中阴离子数目为0.2NA | |
| C. | 标准状况下,2.24 L SO3中含有氧原子数目为0.3NA | |
| D. | 2 g D216O中含中子、质子、电子数目均为NA |
 A、B、C、D、E五种元素的元素序数依次增大.A的原子序数等于周期数;B的最外层电子数是次外层电子数的2倍,D的L层有两对成对电子;E+的核外有三个电子层,且都处于全满状态.试回答下列问题:
A、B、C、D、E五种元素的元素序数依次增大.A的原子序数等于周期数;B的最外层电子数是次外层电子数的2倍,D的L层有两对成对电子;E+的核外有三个电子层,且都处于全满状态.试回答下列问题: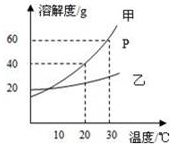 如图是甲、乙两种固体物质的溶解度曲线.据图回答:
如图是甲、乙两种固体物质的溶解度曲线.据图回答: