题目内容
9.已知A的产量可以衡量一个国家石油化工发展的水平,F主要存在于植物的细胞壁、棉花、木材中的一种天然高分子 化合物.有关物质的转化关系如图所示(部分反应条件、产物省略);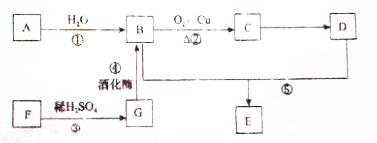
(1)C中官能团的名称:醛基
(2)A到B的化学反应方程式:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH
(3)下列说法正确的是:D
A.往F水解后的溶液中加入新制氢氧化铜,加热后未出现砖红色沉淀,则F未水解;
B.A使酸性高锰酸钾溶液褪色和溴水褪色的原理相同;
C.E在碱性溶液中 的水解反应也称为皂化反应;
D.反应③与反应⑤的反应类型相同.
分析 A的产量可以衡量一个国家石油化工发展的水平,则A为C2H4,F主要存在于植物的细胞壁、棉花、木材中的一种天然高分子化合物,同F为纤维素,根据各物质的转化关系及反应条件可知,F在稀硫酸条件下水解得G为C6H12O6,A与水加成得B为CH3CH2OH,乙醇在Cu作催化剂条件下发生氧化反应生成C为CH3CHO,CH3CHO可进一步氧化生成D为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成乙酸乙酯,故E为CH3COOCH2CH3,据此答题.
解答 解:A的产量可以衡量一个国家石油化工发展的水平,则A为C2H4,F主要存在于植物的细胞壁、棉花、木材中的一种天然高分子化合物,同F为纤维素,根据各物质的转化关系及反应条件可知,F在稀硫酸条件下水解得G为C6H12O6,A与水加成得B为CH3CH2OH,乙醇在Cu作催化剂条件下发生氧化反应生成C为CH3CHO,CH3CHO可进一步氧化生成D为CH3COOH,CH3CH2OH和CH3COOH在浓硫酸作用下反应生成乙酸乙酯,故E为CH3COOCH2CH3,
(1)C为CH3CHO,C中官能团的名称为醛基,故答案为:醛基;
(2)A到B的化学反应方程式为CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,故答案为:CH2=CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;
(3)A.往F水解后的溶液呈酸性,所以加入新制氢氧化铜,加热后未出现砖红色沉淀,不能说明F未水解,故A错误;
B.A使酸性高锰酸钾溶液褪色是被氧化,和溴水褪色是发生加成反应,所以原理有相同,故B错误;
C.高级酯肪酸甘油酯的碱性水解才称为皂化反应,故C错误;
D.反应③与反应⑤都取代反应,故D正确,
故选D.
点评 本题考查有机物推断,涉及烯、醇、醛、羧酸之间的转化关系,难度不大,注意基础知识的理解掌握.

 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案| A. | Ba(OH)2 | B. | Na2O2 | C. | SiO2 | D. | Fe2O3 |
| A. | 在常温常压下,11.2L Cl2含有的分子数为0.5NA | |
| B. | 在常温常压下,25.5g NH3所含的原子数为6NA | |
| C. | 标准状况下,11.2L水所含的分子数为0.5NA | |
| D. | 在同温同压下,相同体积的任何气体单质所含的原子数相同 |
| A. | +8 | B. | +3 | C. | +6 | D. | +2 |
| A. | 100 mL 1 mol/L的盐酸中含HCl分子数为0.1NA | |
| B. | 7.8 g Na2O2和Na2S的混合物中阴离子数目为0.2NA | |
| C. | 标准状况下,2.24 L SO3中含有氧原子数目为0.3NA | |
| D. | 2 g D216O中含中子、质子、电子数目均为NA |
| A. | 4:5 | B. | 2:7 | C. | 2:5 | D. | 2:9 |
| A. | 锅炉水垢用Na2CO3溶液浸泡一段时间后,可用盐酸溶解 | |
| B. | 向Mg(OH)2悬浊液中滴加FeCl3溶液,固体颜色变深 | |
| C. | NaH2PO4溶液显酸性,Na2HPO4溶液显碱性,两种溶液中都有电离平衡和水解平衡 | |
| D. | 等物质的量浓度的(NH4)2CO3,(NH4)2SO4,(NH4)2Fe(SO4)2三种溶液,NH${\;}_{4}^{+}$浓度相等 |
 氧化铜是一种黑色粉末,可作玻璃和瓷器着色剂、油类的脱硫剂、有机合成的催化剂.为获得纯净的氧化铜以探究其性质,某化学兴趣小组利用废旧印刷电路板获得氧化铜,实现资源再生,并减少污染.
氧化铜是一种黑色粉末,可作玻璃和瓷器着色剂、油类的脱硫剂、有机合成的催化剂.为获得纯净的氧化铜以探究其性质,某化学兴趣小组利用废旧印刷电路板获得氧化铜,实现资源再生,并减少污染.(1)获得硫酸铜:该小组同学利用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜,从而获得硫酸铜,写出该反应的离子方程式:Cu+2H++H2O2═Cu2++2H2O.
(2)制备氧化铜:
粗CuSO4溶液(含有硫酸铁杂质)$\stackrel{步骤Ⅰ}{→}$纯CuSO4溶液$\stackrel{步骤Ⅱ}{→}$CuSO4•5H2O→…→CuO
已知:pH≥6.4时Cu(OH)2沉淀完全,而在pH=3~4时Fe(OH)3即能完全沉淀.
①步骤Ⅰ的目的是除去硫酸铁,可慢慢加入下列某些物质,搅拌,以控制溶液pH=3.5.加热煮沸一段时间,过滤,用稀硫酸酸化滤液至PH=1.下列物质有利于控制溶液PH=3.5的是AC.
A.Cu2(OH)2CO3粉末 B.Fe2O3粉末
C.Cu(OH)2固体 D.NaOH固体
②步骤Ⅱ的目的是得到CuSO4•5H2O固体,操作是蒸发浓缩、冷却结晶、过滤、水浴加热烘干.水浴加热的特点是受热更均匀,温度不会超过100℃.
(3)探究氧化铜的性质
探究氧化铜是否能加快氯酸钾的分解,并与二氧化锰的催化效果进行比较.用如图装置进行实验,实验时均以收集25mL气体为准,其他可能影响实验的因素均已忽略,相关数据见表:
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| KClO3质量 | 1.2g | 1.2g | 1.2g |
| 其他物质质量 | 无其他物质 | CuO 0.5g | MnO2 0.5g |
| 待测数据 |
②如何检查该装置的气密性:上下移动量气管,使量气管液出现高度差,一段时间后量气管中的液面差不变,则装置不漏气.
③为探究CuO在实验Ⅱ中是否起催化作用,需补做如下实验(无需写出具体操作):
a.检测CuO反应前后质量是否改变,b.CuO的化学性质有没有改变.