题目内容
胶体是一种重要的分散系.
(1)制备Fe(OH)3胶体是向煮沸的蒸馏水中逐滴加入 溶液,继续煮沸至 ,停止加热.
(2)向Fe(OH)3胶体中加入某种溶液,出现沉淀,继续滴加该溶液后沉淀溶解.滴入的溶液可能是 .
A.NaOH溶液 B.稀H2SO4 C.Na2SO4溶液 D.乙醇溶液
(3)区分胶体和溶液常用的方法叫做 ,这是因为胶体粒子对光线的 作用而形成的.
(1)制备Fe(OH)3胶体是向煮沸的蒸馏水中逐滴加入
(2)向Fe(OH)3胶体中加入某种溶液,出现沉淀,继续滴加该溶液后沉淀溶解.滴入的溶液可能是
A.NaOH溶液 B.稀H2SO4 C.Na2SO4溶液 D.乙醇溶液
(3)区分胶体和溶液常用的方法叫做
考点:胶体的重要性质
专题:溶液和胶体专题
分析:(1)根据制取胶体的实验分析;
(2)根据胶体的聚沉及氢氧化铁的性质分析;
(3)胶体和溶液是不同的分散系,胶体有丁达尔效应溶液没有.
(2)根据胶体的聚沉及氢氧化铁的性质分析;
(3)胶体和溶液是不同的分散系,胶体有丁达尔效应溶液没有.
解答:
解:(1)向沸水中滴入几滴FeCl3饱和溶液,继续煮沸至溶液变成红褐色,即可制得氢氧化铁胶体,
故答案为:FeCl3饱和溶液,溶液呈红褐色;
(2)向制得Fe(OH)3 胶体中加入硫酸,胶体会发生聚沉,Fe(OH)3能溶于硫酸,所以沉淀又消失,沉淀溶解的离子方程式为:Fe(OH)3+3H+=Fe3++3H2O;故答案为:B;
(3)胶体具有丁达尔效应,这是因为胶体粒子对光线的散射作用而形成的,区分胶体和溶液常用的方法叫做丁达尔效应,
故答案为:丁达尔效应;散射.
故答案为:FeCl3饱和溶液,溶液呈红褐色;
(2)向制得Fe(OH)3 胶体中加入硫酸,胶体会发生聚沉,Fe(OH)3能溶于硫酸,所以沉淀又消失,沉淀溶解的离子方程式为:Fe(OH)3+3H+=Fe3++3H2O;故答案为:B;
(3)胶体具有丁达尔效应,这是因为胶体粒子对光线的散射作用而形成的,区分胶体和溶液常用的方法叫做丁达尔效应,
故答案为:丁达尔效应;散射.
点评:本题考查胶体制备、性质的知识,注意把握相关物质的性质,难度不大.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
设NA表示阿伏伽德罗常数值,下列叙述正确的是( )
| A、常温下,1L pH=12的Ba(OH)2溶液中含有的OH-数为0.01NA |
| B、常温下,1L 0.1mol/L的CH3COOH溶液中含有的H+数为0.1NA |
| C、11.2 L乙烯、乙烷的混合气体中含有的碳原子数为NA |
| D、5.6 g Fe和足量盐酸完全反应,转移的电子数为0.3NA |
五种短周期元素(用字母表示)在周期表中的相对位置如表,其中R原子中最外层电子数是最内层电子数的3倍.下列判断正确的是( )
| X | Y | ||
| Z | M | R |
| A、气态氢化物稳定性:X>Y |
| B、最高价氧化物的水化物的酸性:Y>M |
| C、Z单质是一种常用的半导体材料 |
| D、Z、M、R的原子半径依次增大,最高化合价依次升高 |
下列各组中属于同位素关系的是( )
| A、16O和18O |
| B、T2O与H2O |
| C、24Mg和24Na |
| D、金刚石与石墨 |
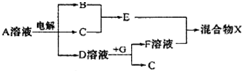
 A、B、C、D、E、F六种元素位于周期表前四周期且原子序数依次增大.①A元素的一种核素中子数是质子数的2倍;②基态B原子核外有两个未成对电子;③大气中C的游离态含量最高;④D原子基态核外电子运动状态共8种;⑤E、F原子序数相差3,基态E原子中有4个未成对屯子且全在同一能级内.
A、B、C、D、E、F六种元素位于周期表前四周期且原子序数依次增大.①A元素的一种核素中子数是质子数的2倍;②基态B原子核外有两个未成对电子;③大气中C的游离态含量最高;④D原子基态核外电子运动状态共8种;⑤E、F原子序数相差3,基态E原子中有4个未成对屯子且全在同一能级内.