题目内容
实验室制取H2的反应方程式为:Zn+H2SO4═ZnSO4+H2↑.
(1) 是氧化剂; 是还原剂; 元素被氧化; 元素被还原; 是氧化产物; 是还原产物.
(2)用双线桥表示出该反应电子转移的方向和数目 :Zn+H2SO4═ZnSO4+H2.
(1)
(2)用双线桥表示出该反应电子转移的方向和数目
考点:氧化还原反应,氧化还原反应的电子转移数目计算
专题:氧化还原反应专题
分析:反应Zn+H2SO4═ZnSO4+H2↑中,Zn元素化合价升高,被氧化,为还原剂,H元素化合价降低,被还原,H2SO4为氧化剂,以此解答该题.
解答:
解:(1)反应Zn+H2SO4═ZnSO4+H2↑中,Zn元素化合价升高,被氧化,Zn为还原剂,H元素化合价降低,被还原,H2SO4为氧化剂,ZnSO4为氧化产物,H2为还原产物,
故答案为:H2SO4;Zn;Zn;H;ZnSO4;H2.
(2)该反应中转移的电子数为2e-,电子转移的方向和数目为 ,
,
故答案为: .
.
故答案为:H2SO4;Zn;Zn;H;ZnSO4;H2.
(2)该反应中转移的电子数为2e-,电子转移的方向和数目为
 ,
,故答案为:
 .
.
点评:本题考查氧化还原反应,为高考常见题型,侧重基本概念的考查,注意把握反应中元素的化合价变化为解答的关键,题目难度不大.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
下列实验操作或对实验事实的描述不正确的有 ( )
| A、用托盘天平称量17.55g氯化钠晶体 |
| B、碳酸钠溶液保存在带玻璃塞的试剂瓶 |
| C、用干燥的pH试纸测定新制氯水的pH |
| D、使用容量瓶配制溶液时,俯视刻度线定容后浓度偏大 |
| E、向饱和FeCl3溶液中滴加少量NaOH溶液,可制取Fe(OH)3胶体 |
| F、除去CO2气体中混有的少量HCl,可以将气体通入饱和碳酸氢钠溶液 |
有七种物质:①甲烷 ②苯 ③聚乙烯 ④乙炔 ⑤1-丁烯 ⑥环己烷 ⑦甲苯,其中既能使酸性高锰酸钾溶液褪色,又能使溴水因发生反应而褪色的是( )
| A、①④⑤ | B、④⑤ |
| C、④⑤⑦ | D、③④⑤ |
用VSEPR模型预测,下列分子形状与H2O相似,都为V型的是( )
| A、OF2 |
| B、BeCl2 |
| C、SO2 |
| D、CO2 |
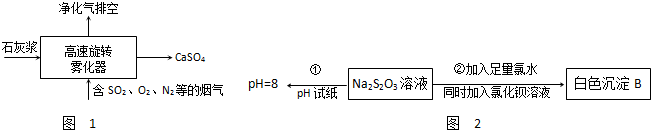
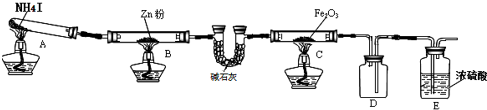
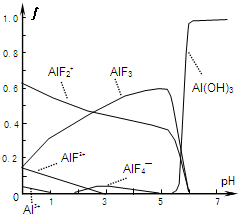 Ⅰ.氟和氟盐是化工原料.由于氟气性质活泼,很晚才制取出来.(1)不能通过电解纯净的液态HF获得F2,其原因是
Ⅰ.氟和氟盐是化工原料.由于氟气性质活泼,很晚才制取出来.(1)不能通过电解纯净的液态HF获得F2,其原因是