题目内容
水是人类生存和发展的宝贵资源,而水质的污染问题却越来越严重.目前,世界各国已高度重视这个问题,并采取积极措施进行治理.
(1)工业废水中常含有不同类型的污染物,可采用不同的方法处理.以下处理措施和方法都正确的是 (填字母编号,可多选).
(2)如图是某市污水处理的工艺流程示意图:
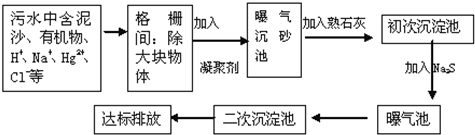
①下列物质中不可以作为混凝剂(沉降剂)使用的是 (填字母编号,可多选).
A.偏铝酸钠 B.氧化铝 C.碱式氯化铝 D.氯化铁
②混凝剂除去悬浮物质的过程是 (填字母编号).
A.只是物理过程 B.只是化学过程 C.是物理和化学过程
(3)在氯氧化法处理含CN一的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质.某厂废水中含KCN,其浓度为650mg?L-1.现用氯氧化法处理,发生如下反应:
KCN+2KOH+Cl2=KOCN+2KCl+H2O 再投入过量液氯,可将氰酸盐进一步氯化为氮气.请配平下列化学方程式:口KOCN+口KOH+口Cl2→口CO2+口N2+口KCl+口H2O若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯 g.
(1)工业废水中常含有不同类型的污染物,可采用不同的方法处理.以下处理措施和方法都正确的是
| 选项 | 污染物 | 处理措施 | 方法类别 |
| A | 废酸 | 加生石灰中和 | 物理法 |
| B | Cu2+等重金属离子 | 加硫酸盐沉降 | 化学法 |
| C | 含纯碱的废水 | 加石灰水反应 | 化学法 |

①下列物质中不可以作为混凝剂(沉降剂)使用的是
A.偏铝酸钠 B.氧化铝 C.碱式氯化铝 D.氯化铁
②混凝剂除去悬浮物质的过程是
A.只是物理过程 B.只是化学过程 C.是物理和化学过程
(3)在氯氧化法处理含CN一的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质.某厂废水中含KCN,其浓度为650mg?L-1.现用氯氧化法处理,发生如下反应:
KCN+2KOH+Cl2=KOCN+2KCl+H2O 再投入过量液氯,可将氰酸盐进一步氯化为氮气.请配平下列化学方程式:口KOCN+口KOH+口Cl2→口CO2+口N2+口KCl+口H2O若处理上述废水20L,使KCN完全转化为无毒物质,至少需液氯
考点:常见的生活环境的污染及治理,氧化还原反应
专题:
分析:(1)污染治理要求能除掉有毒的物质,新生成的物质对环境无污染,物理法与化学法的区别是否有新物质生成;
(2)①水解生成胶体的可作为混凝剂;
②生成胶体为化学变化,而具有吸附性为物理变化,胶体聚沉为物理变化;
(3)KOCN+KOH+Cl2→CO2+N2+KCl+H2O中,N元素化合价由-3价升高为0价,Cl元素化合价由0价降低为-1价,结合电子守恒及原子守恒配平;计算废水中KCN的质量,再根据n=
计算KCN的物质的量,由电子转移守恒计算n(Cl2),再根据m=nM计算需要氯气的质量.
(2)①水解生成胶体的可作为混凝剂;
②生成胶体为化学变化,而具有吸附性为物理变化,胶体聚沉为物理变化;
(3)KOCN+KOH+Cl2→CO2+N2+KCl+H2O中,N元素化合价由-3价升高为0价,Cl元素化合价由0价降低为-1价,结合电子守恒及原子守恒配平;计算废水中KCN的质量,再根据n=
| m |
| M |
解答:
解:A、酸和碱的中和反应为化学反应,为化学法,故A错误;
B.硫酸铜可溶,所以不能沉淀除去,故B错误;
C.含纯碱的废水,加石灰水反应生成生成沉淀,为化学方法,故C正确;
故答案为:C;
(2)①工艺中的混凝剂常用明矾,则水解生成胶体的可作为混凝剂,ACD中物质均可水解生成胶体,只有B中氧化铝不溶于水,不能作混凝剂,故答案为:B;
②生成胶体为化学变化,而具有吸附性为物理变化,胶体聚沉为物理变化,则混凝剂除去悬浮物质的过程是物理和化学过程,故答案为:C;
(3)KOCN+KOH+Cl2→CO2+N2+KCl+H2O中,N元素化合价由-3价升高为0价,Cl元素化合价由0价降低为-1价,由电子守恒及原子守恒可知,该反应为2KOCN+4KOH+3Cl2=2CO2+N2↑+6KCl+2H2O,废水中KCN的质量
=0.2mol,再根据n=
计算KCN的物质的量,由KCN+2KOH+Cl2=KOCN+2KCl+H2O、2KOCN+4KOH+3Cl2=2CO2+N2↑+6KCl+2H2O可知,使KCN完全转化为无毒物质,应生成CO、N2,整个过程中C元素化合价由+2价升高为+4价,N元素化合价由-3价升高为0价,Cl元素化合价由0价降低为-1价,遵循电子转移守恒,则2×n(Cl2)=0.2mol×(4-2)+0.2mol×[0-(-3)],解得n(Cl2)=0.5mol,故需要氯气的质量为0.5mol×71g/mol=35.5g,
故答案为:2;4;3;2;1;6;2;35.5.
B.硫酸铜可溶,所以不能沉淀除去,故B错误;
C.含纯碱的废水,加石灰水反应生成生成沉淀,为化学方法,故C正确;
故答案为:C;
(2)①工艺中的混凝剂常用明矾,则水解生成胶体的可作为混凝剂,ACD中物质均可水解生成胶体,只有B中氧化铝不溶于水,不能作混凝剂,故答案为:B;
②生成胶体为化学变化,而具有吸附性为物理变化,胶体聚沉为物理变化,则混凝剂除去悬浮物质的过程是物理和化学过程,故答案为:C;
(3)KOCN+KOH+Cl2→CO2+N2+KCl+H2O中,N元素化合价由-3价升高为0价,Cl元素化合价由0价降低为-1价,由电子守恒及原子守恒可知,该反应为2KOCN+4KOH+3Cl2=2CO2+N2↑+6KCl+2H2O,废水中KCN的质量
| 13g |
| 65g/mol |
| m |
| M |
故答案为:2;4;3;2;1;6;2;35.5.
点评:本题考查较综合,涉及环境污染及治理、氧化还原反应及计算,侧重高频考点的考查,注意(3)中电子守恒的应用,综合性较强,题目难度中等.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
某温度下将N2和H2充入一恒容的密闭容器中,发生反应:N2+3H2?2NH3,某一时刻用下列各组内两种物质表示的该反应速率,其中正确的是( )
| A、v(N2)=0.01 mol?(L?s)-1,v(H2)=0.02 mol?(L?s)-1 |
| B、v(H2)=0.02 mol?(L?s)-1,v(NH3)=0.02 mol?(L?s)-1 |
| C、v(N2)=0.01 mol?(L?s)-1,v(NH3)=0.03 mol?(L?s)-1 |
| D、v(H2)=0.06 mol?(L?s)-1,v(NH3)=0.04 mol?(L?s)-1 |
下列各组微粒具有相同的质子数和电子数的是( )
| A、OH-、H2O |
| B、NH4+、NH2- |
| C、H3O+、CH4 |
| D、HCl、F2 |
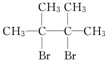
下列化学用语表达正确的是( )
| A、一氯乙烷的结构式CH3Cl |
| B、丁烷的结构简式CH3(CH2)2CH3 |
C、四氯化碳的电子式 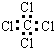 |
D、C2H4分子比例模型: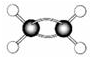 |
 (1)某元素的基态原子最外层电子排布为3s23p2,它的次外层上电子云形状有
(1)某元素的基态原子最外层电子排布为3s23p2,它的次外层上电子云形状有