题目内容
下列离子方程式书写正确的是( )
| A、硫酸亚铁的酸性溶液中加过氧化氢溶液:Fe2++H2O2+2H+═Fe3++2H2O |
| B、NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO3-+Ba2++2OH-=BaCO3↓+2H2O+CO32- |
| C、NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |
| D、Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-═2Fe2++I2 |
考点:离子方程式的书写
专题:离子反应专题
分析:A.电荷不守恒;
B.NaHCO3溶液中加入过量的Ba(OH)2溶液,反应生成碳酸钡和氢氧化钠、水;
C.酸性的高锰酸钾具有强的氧化性,氧化亚硝酸钠;
D.硝酸根离子在酸性环境下具有强的氧化性,能够氧化碘离子.
B.NaHCO3溶液中加入过量的Ba(OH)2溶液,反应生成碳酸钡和氢氧化钠、水;
C.酸性的高锰酸钾具有强的氧化性,氧化亚硝酸钠;
D.硝酸根离子在酸性环境下具有强的氧化性,能够氧化碘离子.
解答:
解:A.硫酸亚铁的酸性溶液中加过氧化氢溶液,离子方程式:2Fe2++H2O2+2H+═2Fe3++2H2O,故A错误;
B.NaHCO3溶液中加入过量的Ba(OH)2溶液,离子方程式:HCO3-+Ba2++OH-=BaCO3↓+H2O,故B错误;
C.NaNO2溶液中加入酸性KMnO4溶液,离子方程式:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O,故C正确;
D.Fe(NO3)3溶液中加入过量的HI溶液,离子方程式:Fe3++3NO3-+12H++10I-=Fe2++5I2+6H2O+3NO↑,故D错误;
故选:C.
B.NaHCO3溶液中加入过量的Ba(OH)2溶液,离子方程式:HCO3-+Ba2++OH-=BaCO3↓+H2O,故B错误;
C.NaNO2溶液中加入酸性KMnO4溶液,离子方程式:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O,故C正确;
D.Fe(NO3)3溶液中加入过量的HI溶液,离子方程式:Fe3++3NO3-+12H++10I-=Fe2++5I2+6H2O+3NO↑,故D错误;
故选:C.
点评:本题考查离子方程式的书写,明确发生的反应并熟悉离子反应方程式的书写方法是解答本题的关键,题目难度不大,注意反应物的用量对反应的影响.

练习册系列答案
相关题目
下列叙述错误的是( )
| A、漂白粉要密闭保存 |
| B、等量的铝分别与足量的盐酸和氢氧化钠溶液反应产生氢气的量相同 |
| C、常温下铁和浓硫酸能发生化学反应 |
| D、工业上用电解氯化铝的方法来制取金属铝 |
下列离子方程式中书写正确的是( )
| A、FeCl2溶液中通入Cl2:Fe2++Cl2═Fe3++2Cl- |
| B、Al2O3与NaOH溶液反应:Al2O3+2OH-═2[Al(OH)4]- |
| C、FeCl3溶液与铜:Fe3++Cu═Fe2++Cu2+ |
| D、用醋酸除水垢:2CH3COOH+CaCO3═2CH3COO-+Ca2++H2O+CO2↑ |
下列叙述正确的是( )
| A、检验Fe(NO3)2试样是否变质:取少量试样加水溶解,用稀H2SO4酸化,滴加KSCN溶液 |
| B、欲鉴别AlC13溶液和AgNO3溶液,向2种待测液中分别滴加足量氨水 |
| C、将溴丙烷与足量氢氧化钠溶液混合加热,冷却后加硝酸银溶液,可检验溴元素 |
| D、用相互滴加的方法鉴别Ca(OH)2和NaHCO3溶液 |
根据相关的化学原理,下列判断正确的是( )
| A、由于水中存在氢键,所以稳定性:H2O>H2S |
| B、由于非金属性F>Cl>Br>I,所以酸性:HF>HCl>HBr>HI |
| C、分散质粒子直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| D、若R2-和M+的电子层结构相同,则原子半径 R>M |
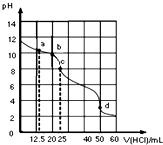 在常温下,0.1000mol?L-1Na2CO3溶液25mL 用0.1000mol?L-1盐酸滴定,其滴定曲线如图.对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是( )
在常温下,0.1000mol?L-1Na2CO3溶液25mL 用0.1000mol?L-1盐酸滴定,其滴定曲线如图.对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是( )| A、a点:c(CO32-)=c(HCO3-)>c(OH-) |
| B、b点:5c(Cl-)=4c(HCO3-a点:c(CO32-)=c(HCO3-)>c(OH-))+4c(CO32-) |
| C、c点:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
| D、d点:c(Na+)<c(Cl-)+ |
下列图示与对应的叙述相符的是( )
A、 说明烯烃与H2的加成反应是放热反应,虚线表示在有催化剂的条件下进行 |
B、 用0.1000mol/LNaOH溶液分别滴定浓度相同的三种一元酸,由图曲线可确定①的酸性最强 |
C、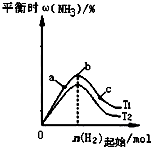 图表示合成氨反应在其他条件不变的情况下,改变n(H2)起始对平衡的影响.由此可知,N2的转化率最高的是b点;且T1>T2,K2>K1(T1和T2表示温度,K1、K2表示对应温度下的平衡常数) |
D、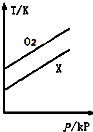 在体积相同的两个密闭容器中,分别充入等质量的O2和X气体,由图可确定X可能是CH4 |
下列各组离子在指定溶液中能大量共存的是( )
| A、无色溶液中:K+、Na+、MnO4-、SO42- |
| B、酸性溶液中:Cl-、Na+、AlO2-、NO3- |
| C、加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+ |
| D、有较多Fe3+的溶液中:Na+、NH4+、Cl-、SO42- |
