题目内容
某有机物其结构简式如图关于该有机物,下列叙述不正确的是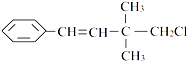 ( )
( )
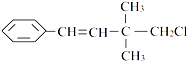 ( )
( )| A、一定条件下,能发生加聚反应 |
| B、能使溴水褪色 |
| C、一定条件下,能发生取代反应 |
| D、能与NaOH的醇溶液共热发生消去反应 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:有机物含有碳碳双键,可发生加成、加聚和氧化发硬,含有氯原子,可发生取代反应,以此解答该题.
解答:
解:A.有机物含有碳碳双键,可发生加聚反应,故A正确;
B.含有碳碳双键,可发生加成反应,能使溴水褪色,故B正确;
C.含有氯原子,能发生水解,也为取代反应,故C正确;
D.氯原子相邻的碳原子没有氢原子,不能发生消去反应,故DD错误.
故选D.
B.含有碳碳双键,可发生加成反应,能使溴水褪色,故B正确;
C.含有氯原子,能发生水解,也为取代反应,故C正确;
D.氯原子相邻的碳原子没有氢原子,不能发生消去反应,故DD错误.
故选D.
点评:本题考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,注意把握有机物的结构和官能团的性质,为解答该类题目的关键,难度不大.

练习册系列答案
相关题目
某主族元素原子的第一、二、三、四各级电离能依次为:899KJ/mol、1757KJ/mol、14840KJ/mol、18025KJ/mol,试分析该元素所在的族序数为( )
| A、IA族 | B、ⅡA族 |
| C、ⅢA族 | D、IVA族 |
以下各微粒中,所有原子或离子不满足最外层都为8电子结构的是( )
| A、Na2O2 |
| B、PCl3 |
| C、CCl4 |
| D、BF3 |
C和CuO在高温下反应可能生成Cu、Cu2O、CO2、CO.现将1g碳粉跟8g CuO混合,在硬质试管中隔绝空气高温加热,将生成的气体全部通入足量NaOH溶液中,并收集残余的气体,测得溶液增加的质量为1.1g,残余气体在标准状况下的体积为560mL.下列说法错误的是( )
| A、在硬质试管中隔绝空气高温加热固体混合物时,有0.6 g碳参加了反应 |
| B、试管中发生的所有氧化还原反应共转移电子0.15 mol |
| C、反应后试管中剩余的固体混合物的总质量为7.2 g |
| D、反应生成铜和氧化亚铜的总物质的量为0.1 mol |
下列实验能达到相应目的是( )
A、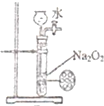 制备少量的氧气 |
B、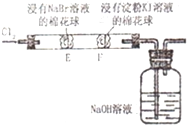 证明氧化性Cl2>Br2>I2 |
C、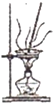 将海带灼烧成灰 |
D、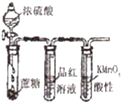 说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性 |
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A、0.2mol/LCH3COONa与0.1mol/LHCl溶液等体积混合(pH<7):c(Na+)>c(CH3COO-)>c(Cl-)>c(H+)>c(OH-) |
| B、0.1mol/LNH4Cl与0.1mol/L氨水等体积混合(pH>7):c(NH3?H2O)>c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| C、0.1mol/LNa2C2O4与0.1mol/LHCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
| D、0.1mol/LNa2CO3与0.2mol/L NaHCO3溶液等体积混合:3c(Na+)=4[c(CO32-)+c(HCO3-)+c(H2CO3)] |
为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位同学分别设计了如下四个实验,你认为结论不正确的是( )
| A、将铜片放入稀硫酸中,无现象.若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气生成 |
| B、将除去氧化膜的相同大小、相同质量的镁条和铝条与相同浓度盐酸反应,前者速率大于后者 |
| C、两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 |
| D、相同条件下等质量的块状和粉末状大理石与相同浓度盐酸反应时,粉末状的反应速率快 |