题目内容
8.4-羟基扁桃酸可用于制备抗生素及血管扩张类的药物,香豆素-3-羧酸可用于制造香料,二者合成路线如下(部分产物及条件未列出):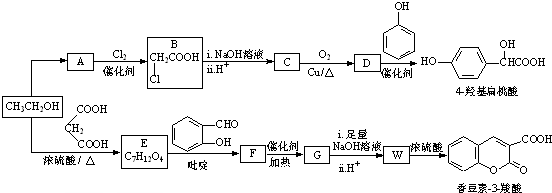
已知:
Ⅰ.RCOOR′+R″OH$→_{加热}^{催化剂}$RCOOR″+R′OH
Ⅱ.
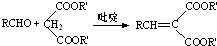 (R,R′,R″表示氢、烷基或芳基)
(R,R′,R″表示氢、烷基或芳基)(1)A相对分子质量为60,A的结构简式是CH3COOH.
(2)A→B的反应类型是取代反应.
(3)C中含氧官能团的名称是羧基、羟基.
(4)D→4-羟基扁桃酸的化学方程式是OHC-COOH+
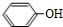 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$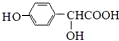 .
.(5)E→F的化学方程式是C2H5OOC-CH2-COOC2H5+
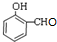 $\stackrel{吡啶}{→}$
$\stackrel{吡啶}{→}$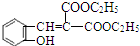 +H2O.
+H2O.(6)关于有机物F下列说法正确的是c.
a.存在顺反异构b.分子中不含醛基 c.能发生加成、水解、取代等反应
(7)写出任意一种符合下列条件的4-羟基扁桃酸 (
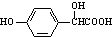 )的同分异构体
)的同分异构体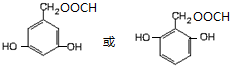 .
.a能发生水解和银镜反应的芳香族化合物
b.1mol该物质最多能与3mol NaOH发生反应
c.核磁共振氢谱显示有五个峰,峰面积之比为1:2:2:2:1
(8)已知G分子中存在两个六元环,由W→香豆素-3-羧酸的化学方程式为
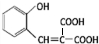 $\stackrel{浓硫酸}{→}$
$\stackrel{浓硫酸}{→}$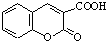 +H2O.
+H2O.
分析 乙醇与丙二酸发生酯化反应生成E,结合E的分子式可知,E的结构简式为C2H5OOC-CH2-COOC2H5,E与 发生信息Ⅱ中反应生成F,F系列反应得到香豆素-3-羧酸,由香豆素-3-羧酸的结构,可知W为
发生信息Ⅱ中反应生成F,F系列反应得到香豆素-3-羧酸,由香豆素-3-羧酸的结构,可知W为 ,则F为
,则F为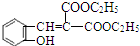 ,F发生信息I中反应生成G,C分子中含有2个六元环,则G为
,F发生信息I中反应生成G,C分子中含有2个六元环,则G为 .A的相对分子质量为60,由ClCH2COOH结构可知乙醇发生氧化反应生成A为CH3COOH,ClCH2COOH与氢氧化钠溶液反应、酸化得到C为HOCH2COOH,C发生催化氧化得到D为OHC-COOH,D与苯酚发生加成反应生成对羟基扁桃酸为
.A的相对分子质量为60,由ClCH2COOH结构可知乙醇发生氧化反应生成A为CH3COOH,ClCH2COOH与氢氧化钠溶液反应、酸化得到C为HOCH2COOH,C发生催化氧化得到D为OHC-COOH,D与苯酚发生加成反应生成对羟基扁桃酸为 ,据此解答.
,据此解答.
解答 解:乙醇与丙二酸发生酯化反应生成E,结合E的分子式可知,E的结构简式为C2H5OOC-CH2-COOC2H5,E与 发生信息Ⅱ中反应生成F,F系列反应得到香豆素-3-羧酸,由香豆素-3-羧酸的结构,可知W为
发生信息Ⅱ中反应生成F,F系列反应得到香豆素-3-羧酸,由香豆素-3-羧酸的结构,可知W为 ,则F为
,则F为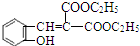 ,F发生信息I中反应生成G,C分子中含有2个六元环,则G为
,F发生信息I中反应生成G,C分子中含有2个六元环,则G为 .A的相对分子质量为60,由ClCH2COOH结构可知乙醇发生氧化反应生成A为CH3COOH,ClCH2COOH与氢氧化钠溶液反应、酸化得到C为HOCH2COOH,C发生催化氧化得到D为OHC-COOH,D与苯酚发生加成反应生成对羟基扁桃酸为
.A的相对分子质量为60,由ClCH2COOH结构可知乙醇发生氧化反应生成A为CH3COOH,ClCH2COOH与氢氧化钠溶液反应、酸化得到C为HOCH2COOH,C发生催化氧化得到D为OHC-COOH,D与苯酚发生加成反应生成对羟基扁桃酸为 .
.
(1)由上述分析可知,A的结构简式是CH3COOH,故答案为:CH3COOH;
(2)A生成的ClCH2COOH反应属于取代反应,故答案为:取代反应;
(3)C为HOCH2COOH,含氧官能团的名称是:羧基、羟基,故答案为:羧基、羟基;
(4)D→4-羟基扁桃酸的化学方程式是:OHC-COOH+ $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ ,
,
故答案为:OHC-COOH+ $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$ ;
;
(5)E→F的化学方程式是:C2H5OOC-CH2-COOC2H5+ $\stackrel{吡啶}{→}$
$\stackrel{吡啶}{→}$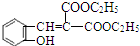 +H2O,
+H2O,
故答案为:C2H5OOC-CH2-COOC2H5+ $\stackrel{吡啶}{→}$
$\stackrel{吡啶}{→}$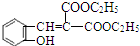 +H2O;
+H2O;
(6)F的结构简式是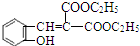 ,
,
a.不饱和碳原子连接2个-COOC2H5,没有顺反异构,故a错误;
b.F分子中不含醛基,故b错误;
c.含有碳碳双键与苯环,可以发生加成反应,含有酯基,可以发生水解反应,酯基、酚羟基均可以发生取代反应,故c正确,
故选:c;
(7)任意一种符合下列条件的4-羟基扁桃酸 (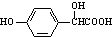 )的同分异构体:a.能发生水解和银镜反应的芳香族化合物,说明含有苯环、酯基、醛基,b.1mol该物质最多能与3mol NaOH发生反应,c.核磁共振氢谱显示有五个峰,峰面积之比为1:2:2:2:1,取代基可以是2个酚羟基、1个-CH2OOCH,可能的结构简式为:
)的同分异构体:a.能发生水解和银镜反应的芳香族化合物,说明含有苯环、酯基、醛基,b.1mol该物质最多能与3mol NaOH发生反应,c.核磁共振氢谱显示有五个峰,峰面积之比为1:2:2:2:1,取代基可以是2个酚羟基、1个-CH2OOCH,可能的结构简式为: ,
,
故答案为: ;
;
(8)由W→香豆素-3-羧酸的化学方程式为: $\stackrel{浓硫酸}{→}$
$\stackrel{浓硫酸}{→}$ +H2O,
+H2O,
故答案为: $\stackrel{浓硫酸}{→}$
$\stackrel{浓硫酸}{→}$ +H2O.
+H2O.
点评 本题考查有机物的推断与合成,需要学生对给予的信息进行利用,较好的考查学生自学能力,注意根据有机物的结构利用正、逆推法相结合进行推断,侧重考查学生分析推理能力,难度中等.

| A. | 7.8gNa2S和Na2O2的混合物中含有的阴离子数目大于0.1NA,小于0.2NA | |
| B. | 常温下0.1mol•L-1的NH4NO3溶液中氮原子数为0.2NA | |
| C. | 标准状况下,2.24L CHCl3的分子数为0.1NA | |
| D. | 19gT35Cl和H37Cl的混合物中所含中子数为10NA |
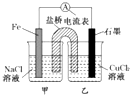
| A. | 原电池的总反应为 Fe+Cu2+=Fe2++Cu | |
| B. | 反应前,电极质量相等,一段时间后,两电极质量相差12g,导线中通过0.2 mol电子 | |
| C. | 其他条件不变,若将CuCl2溶液换为NH4Cl溶液,石墨电极反应式为2H++2e-=H2↑ | |
| D. | 盐桥中是KNO3溶液,则盐桥中NO3-移向乙烧杯 |
(1)他们测硝酸亚铁溶液的pH常温下小于7,用离子方程式解释其原因是Fe2++2H2O?Fe(OH)2+2H+
(2)甲同学欲配制硝酸亚铁溶液,为防止水解,称量一定量硝酸亚铁晶体溶于pH=1的稀硝酸中,溶液呈深棕色,液面上方有红棕色气体,放置一段时间,溶液最终呈黄色.
(已知:Fe2+能与NO结合形成深棕色的[Fe(NO)]2+:Fe2++NO?[Fe(NO)]2+)
①液面上方红棕色气体是NO2
②经检验黄色溶液中有Fe3+.检验Fe3+的操作是取少量黄色溶液于试管中,滴入KSCN溶液,溶液显红色,证明含有Fe3+
③最初溶液中生成[Fe(NO)]2+使溶液呈深棕色,最终溶液变黄色的原因是在稀硝酸中Fe2+被NO3-氧化为Fe3+,使c(Fe2+)降低,Fe2++NO?〔Fe(NO)]2+的平衡向左移动,当Fe2+被完全氧化为Fe3+时,溶液由深棕色变为黄色
(3)甲同学继续用所得溶液进行实验.
| 操作 | 步骤及现象 |
 | i:往溶液中缓慢通入SO2,液面上方有红棕色气体,溶液黄色无明显变化 ii:继续通入足量的SO2,溶液变为深棕色,一段 时间后,溶液变为浅绿色 |
②甲认为由步骤i的现象得出SO2与NO3-发生了反应,没有与Fe3+发生反应,请判断甲的结论是否正确并说明原因:正确,溶液上方产生红棕色的气体,说明NO3-被还原,溶液没有深棕色出现,说明Fe2+没有被氧化为Fe3+
③步骤ii溶液变为浅绿色,反应的离子方程式是2Fe3++SO2+2H2O=2Fe2++SO42-+4H+
④该实验得出的结论是SO2的还原性比Fe2+的强.
(1)如用下图I装置制取氨气,锥形瓶中可选择的试剂是氢氧化钠固体(或浓氨水与碱石灰或浓氨水与生石灰)等.
(2)制备氨基甲酸铵的装置如图Ⅱ所示,把NH3和CO2通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵的小晶体悬浮在CCl4中.当悬浮物较多时,停止制备.
干燥的NH3液体石蜡鼓泡瓶电动搅拌器ⅢCCl4尾气处理冰水液体石蜡鼓泡瓶干燥的CO2
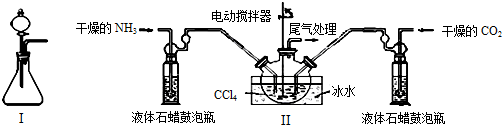
注:CCl4与液体石蜡均为惰性介质.
①图I中滴加液体的仪器名称是分液漏斗,液体石蜡鼓泡瓶的作用是通过观察气泡,调节NH3与CO2通入比例(或通过观察气泡,控制NH3与CO2的反应速率),发生器用冰水冷却的原因是降低温度,提高反应物转化率(或降低温度,防止因反应放热造成产物分解).
②从反应后的混合物中分离出产品的实验方法是过滤(填写操作名称),为了得到干燥产品,应采取的方法是b(填写选项序号).
a.常压加热烘干b.减压40℃以下烘干c.高压加热烘干
(3)制得的氨基甲酸铵可能含有碳酸氢铵、碳酸铵中的一种或两种.
①设计方案,进行成分探究,请填写表中空格.限选试剂:蒸馏水、稀HNO3、BaCl2溶液、Ba(OH)2溶液、AgNO3溶液、稀盐酸.
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量固体样品于试管中,加入蒸馏水至固体溶解. | 得到无色溶液 |
| 步骤2:向试管中加入过量的BaCl2溶液,静置. | 溶液变浑浊,则证明固体中含有(NH4)2CO3. |
| 步骤3:取步骤2的上层清液于试管中加入少量的Ba(OH)2溶液. | 溶液不变浑浊,则证明固体中不含有NH4HCO3. |
| A. | 200 g 63%的浓硝酸中含氧原子个数为6NA | |
| B. | 50mL12mol•L-1盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 若CH3COONa溶液中CH3COO-的数目为6NA,则Na+的数目大于6NA |
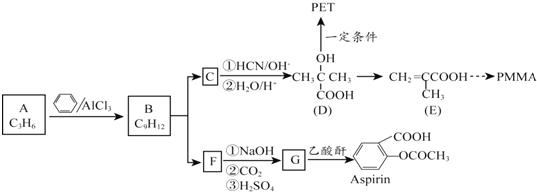
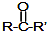 $→_{②H_{2}O/H+}^{①HCN/OH-}$
$→_{②H_{2}O/H+}^{①HCN/OH-}$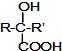
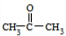 .
.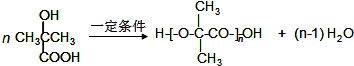 .
.
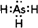 .
.