题目内容
18.下列说法正确的是( )| A. | 无色溶液中滴加盐酸酸化的BaCl2溶液,产生白色沉淀,则溶液中一定含有SO42- | |
| B. | 用加热法可除去NaHCO3中少量的Na2CO3 | |
| C. | 浓硝酸保存在棕色试剂瓶中 | |
| D. | 酸碱中和滴定时,锥形瓶需用待测液润洗后,再加入待测液 |
分析 A.生成的白色沉淀可能为氯化银,原溶液中可能含有银离子;
B.加热后碳酸氢钠分解生成碳酸钠,违反达到除杂的密度;
C.浓硝酸见光易分解,需要用棕色试剂瓶保存;
D.锥形瓶不能润洗,否则会导致待测液中含有溶质的物质的量偏大,测定结果偏高.
解答 解:A.无色溶液中滴加盐酸酸化的BaCl2溶液,产生白色沉淀,该沉淀可能为AgCl,原溶液中不一定含有SO42-,故A错误;
B.若加碳酸氢钠和碳酸钠的混合物,得到的是碳酸钠,违反用加热法可除去NaHCO3中少量的Na2CO3,故B错误;
C.浓硝酸见光分解,需要保存在棕色试剂瓶中,故C正确;
D.酸碱中和滴定时,锥形瓶不能润洗,若锥形瓶需用待测液润洗后再加入待测液,导致待装液中含有溶质的物质的量偏大,消耗标准液体积偏大,则测定结果偏高,故D错误;
故选C.
点评 本题考查较为综合,涉及离子的检验方法、物质的分离与提纯、中和滴定、药品的保存等知识,明确常见元素及其化合物性质为解答关键,注意掌握物质分离与提纯原则,试题培养了学生的灵活应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.下列化学用语正确的是( )
①OH-的电子式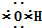
②乙烯的结构简式:CH2=CH2
③甲烷的结构式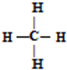
④乙烯的结构式:C2H4.
①OH-的电子式
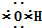
②乙烯的结构简式:CH2=CH2
③甲烷的结构式
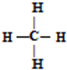
④乙烯的结构式:C2H4.
| A. | ①④ | B. | ②④ | C. | ②③ | D. | ①② |
9.下列有机物溶液在适量的浓度时,不能用于杀菌消毒的是( )
| A. | 苯酚溶液 | B. | 乙醇溶液 | C. | 福尔马林 | D. | 乙酸乙酯溶液 |
3.鉴别下列各组物质,选用的试剂或方法错误的是( )
| 选项 | 要鉴别的物质组 | 试剂 | 方法 |
| A | NaCl/Na2CO3 | BaCl2溶液 | 观察是否产生沉淀 |
| B | NO2/Br2 | 湿润的淀粉碘化钾试纸 | 观察试纸是否变蓝色 |
| C | 乙醇/乙酸 | 新制氢氧化铜悬浊液 | 观察溶液是否变澄清 |
| D | CO2/SO2 | 品红溶液 | 观察溶液红色是否退去 |
| A. | A | B. | B | C. | C | D. | D |
1.下面为钠及其化合物相关的实验报告,请根据题意完成各空白处:
实 验 报 告
(一)实验目的:探究钠及其化合物的有关性质
(二)实验药品及仪器:金属钠,蒸馏水,酒精灯,试管,木条,石棉网,铁架台
(三)实验过程:
(四)实验反思:
(1)钠的化学性质活泼,在自然界中全部以化合态形态(填“游离态”或“化合态”)存在,因此少量钠应保存在煤油中.
(2)写出Na2O2的一种用途:作供氧剂或利用强氧化性杀菌消毒.
实 验 报 告
(一)实验目的:探究钠及其化合物的有关性质
(二)实验药品及仪器:金属钠,蒸馏水,酒精灯,试管,木条,石棉网,铁架台
(三)实验过程:
| 实验步骤 | 实验现象 | 化学方程式或结论 |
| 金属Na长时间放置在空气中 | 银白色的金属光泽消失,迅速变暗,有水珠生成,最终生成白色的粉末 | ①4Na+O2═2Na2O Na2O+H2O═2NaOH 2Na+2H2O═2NaOH+H2↑ 2NaOH+CO2═Na2CO3+H2O |
| 将一块Na置于石棉网上,点燃酒精灯加热 | 钠先熔成小球,剧烈燃烧并发出黄色的火焰,生成②淡黄色色的粉末 | 2Na+O2 ═Na2O2 |
| 往上述生成的 Na2O2上滴加蒸馏水 | 生成的气体能使带火星的木条复燃 | 该气体为③O2 |
(1)钠的化学性质活泼,在自然界中全部以化合态形态(填“游离态”或“化合态”)存在,因此少量钠应保存在煤油中.
(2)写出Na2O2的一种用途:作供氧剂或利用强氧化性杀菌消毒.
18.A+、B2+、C-、D2- 四种离子核外电子排布相同,则这四种离子半径大小顺序是( )
| A. | C->D2->A+>B2+ | B. | B2+>A+>C->D2- | C. | B2+>A+>D2->C- | D. | D2->C->A+>B2+ |
19.在光照条件下,将等物质的量的甲烷和氯气混合充分反应后,得到产物的物质的量最大的是( )
| A. | CH3Cl | B. | CHCl3 | C. | CCl4 | D. | HCl |