题目内容
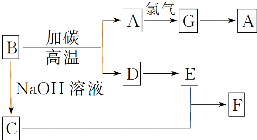 如图是常见物质之间的转化,其中A是芯片的主要成分,其对应的单质的结构与金刚石的结构是相似的,D、E外均含有A的元素.
如图是常见物质之间的转化,其中A是芯片的主要成分,其对应的单质的结构与金刚石的结构是相似的,D、E外均含有A的元素.(1)试推测A
(2)试写出以下的化学方程式,是离子反应的写出离子方程式:B→A
(3)在B+碳→A+D的反应中,碳的作用是
考点:无机物的推断
专题:
分析:A是芯片的主要成分,其对应的单质的结构与金刚石的结构是相似,则A为Si,D、E外均含有A的元素,由转化关系可知,B为SiO2,E为CO,C为Na2SiO3,D为CO,E为CO2,F为H2SiO3,G为SiCl4,据此解答.
解答:
解:A是芯片的主要成分,其对应的单质的结构与金刚石的结构是相似,则A为Si,D、E外均含有A的元素,由转化关系可知,B为SiO2,E为CO,C为Na2SiO3,D为CO,E为CO2,F为H2SiO3,G为SiCl4,
(1)由上述分析可知,A为Si,C为Na2SiO3,F为H2SiO3,故答案为:Si;Na2SiO3;H2SiO3;
(2)B→A是SiO2与碳在高温下反应生成Si和CO,反应的方程式为:SiO2+2C
Si+2CO↑,
C+E→F是硅酸钠溶液与过量二氧化碳反应生成硅酸与碳酸氢钠,反应离子方程式为:SiO32-+2H2O+2CO2═H2SiO3↓+2HCO3-,
故答案为:SiO2+2C
Si+2CO↑;SiO32-+2H2O+2CO2═H2SiO3↓+2HCO3-;
(3)B+碳→A+D的反应为:SiO2+2C
Si+2CO↑,反应中C元素化合价升高,碳其还原剂作用,Si元素化合价由+4降低为0价,当成1 mol Si时,转移电子的物质的量为1mol×4=4mol,
故答案为:4mol.
(1)由上述分析可知,A为Si,C为Na2SiO3,F为H2SiO3,故答案为:Si;Na2SiO3;H2SiO3;
(2)B→A是SiO2与碳在高温下反应生成Si和CO,反应的方程式为:SiO2+2C
| ||
C+E→F是硅酸钠溶液与过量二氧化碳反应生成硅酸与碳酸氢钠,反应离子方程式为:SiO32-+2H2O+2CO2═H2SiO3↓+2HCO3-,
故答案为:SiO2+2C
| ||
(3)B+碳→A+D的反应为:SiO2+2C
| ||
故答案为:4mol.
点评:本题考查无机物的推断,侧重于硅单质及其化合物的考查,注意根据A的用途及晶体结构确定其为Si,再结合转化关系推断,需要学生熟练掌握元素化合物性质,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
将a mL NO,b mL NO2和c mL O2混合于同一试管中,将试管倒置于水中,充分反应后,试管内气体全部消失,则a:b:c不可能是( )
| A、1:1:1 |
| B、2:1:1 |
| C、3:4:7 |
| D、1:5:2 |
某温度下,反应H2(g)+I2(g)?2HI(g);△H>0.在一带有活塞的密闭容器中达到平衡,下列说法中不正确的是( )
| A、恒温,压缩体积,平衡不移动,混合气体颜色加深 |
| B、恒压,充入HI(g),开始时正反应速率减小 |
| C、恒容,升高温度,正反应速率减小 |
| D、恒容,充入H2,I2(g)的体积分数降低 |

 (1)将4molSO2和2molO2充入2L的密闭容器中,在一定条件下发生反应,经10s后达到平衡,测得SO3的浓度为0.6mol?L-1,请回答下列问题:
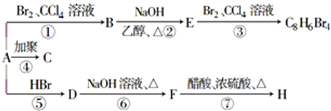
(1)将4molSO2和2molO2充入2L的密闭容器中,在一定条件下发生反应,经10s后达到平衡,测得SO3的浓度为0.6mol?L-1,请回答下列问题: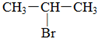 ;1mol某烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如图所示的一系列变化.
;1mol某烃A充分燃烧后可以得到8mol CO2和4mol H2O.该烃A在不同条件下能发生如图所示的一系列变化.