题目内容
19.已知下表为25℃时某些弱酸的电离平衡常数.依据所给信息判断,下列说法正确的是( )| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7Ka2=4.7×10-11 |
| A. | 向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O═2HClO+CO32- | |
| B. | 相同浓度的CH3COONa和NaClO的混合溶液中,c(CH3COOH)+c(HClO)═c(OH-)-c(H+) | |
| C. | 25℃时,0.10mol•L-1Na2CO3溶液通入CO2至溶液的pH=7时,溶液中:c(Na+)═c(CO32-)+c (HCO3-)+c(H2CO3) | |
| D. | 向0.1mol•L-1CH3COONa溶液中加入少量水,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COO)•c(O{H}^{-})}$ 增大 |
分析 A.由表中数据可知酸性CH3COOH>H2CO3>HC1O>HCO3-,结合强酸制取弱酸判断;
B.结合电荷守恒和物料守恒判断;
C.根据NaHCO3溶液呈碱性判断;
D.$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$=$\frac{c(C{H}_{3}CO{O}^{-})c({H}^{+})}{c(C{H}_{3}COOH)•c(O{H}^{-})c({H}^{+})}$=$\frac{Ka}{Kw}$.
解答 解:A.由表中数据可知酸性CH3COOH>H2CO3>HC1O>HCO3-,则碳酸的酸性强于次氯酸,将少量CO2气体通入NaClO溶液中的离子方程式:CO2+H2O+ClO-═HCO3-+HC1O,故A错误;
B.相同浓度的CH3COONa和NaClO的混合溶液中,存在电荷守恒:c(OH-)+c(CH3COO-)+c(ClO-)=c(H+)+c(Na+),物料守恒:c(CH3COOH)+c(CH3COO-)+c(ClO-)+c(HClO)=c(Na+),二者联式可得c(CH3COOH)+c(HClO)═c(OH-)-c(H+),故B正确;
C.如恰好生成NaHCO3,溶液中:c(Na+)═c(CO32-)+c (HCO3-)+c(H2CO3),因NaHCO3溶液呈碱性,则呈中性时,二氧化碳应过量,则c(CO32-)+c (HCO3-)+c(H2CO3)>c(Na+),故C错误;
D.$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$=$\frac{c(C{H}_{3}CO{O}^{-})c({H}^{+})}{c(C{H}_{3}COOH)•c(O{H}^{-})c({H}^{+})}$=$\frac{Ka}{Kw}$,则向0.1mol•L-1CH3COONa溶液中加入少量水,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COO)•c(O{H}^{-})}$ 不变,故D错误.
故选B.
点评 本题考查电解质的强弱与电离常数的关系,为高考常见题型,侧重于学生的分析能力和计算能力的考查,明确酸的电离常数与酸的强弱、酸根离子水解能力的关系是解本题关键,难度中等,注意理解电荷守恒、物料守恒的运用.

 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案| A. | PH=4.3的CH3COOH与CH3COONa混合溶液中:c(Na+)<c(CH3COO-) | |
| B. | NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 | |
| C. | 若Ksp(AgCl)>Ksp(Ag2CrO4),则AgCl 的溶解度大于Ag2CrO4的溶解度 | |
| D. | 向醋酸溶液中加少量水稀释后,溶液中 c(CH3COOH)增大 |
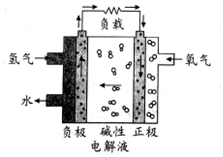
| A. | 通入氢气的电极发生氧化反应 | |
| B. | 正极的电极反应式为O2+2H2O+4e-═4OH- | |
| C. | 碱性电解液中阳离子向通入氢气的方向移动 | |
| D. | 放电过程中碱性电解液的pH不变 |
| A. | 分散系中分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 | |
| B. | 能自发进行的化学反应,一定是△H<0、△S>0 | |
| C. | 将碳酸钠溶液和碳酸氢钠溶液分别蒸干并灼烧,所得固体的成分均为氢氧化钠 | |
| D. | 牺牲阳极的阴极保护法和外加直流电源的阴极保护法都是应用电解原理 |
| A. | 64gCaC2中含有的共用电子对数为3NA | |
| B. | 常温常压下,1.8g甲基(-CD3)中含有的中子数为NA | |
| C. | 1.5mol的MnO2粉末与足量浓盐酸共热转移电子数目小于3NA | |
| D. | 1L0.01 mol•L-1CKA1(SO4)2溶液中含有的阳离子数为0.02NA |
| A. | 蔗糖 | B. | 亚硝酸钠 | C. | AD 钙奶 | D. | 苏丹红 |