题目内容
6.下列表示对应化学反应的离子方程式正确的是( )| A. | 用氯化铁溶液腐蚀铜板:Cu+Fe3+═Cu2++Fe2+ | |
| B. | 碘水中通入适量的SO2:I2+SO2+2H2O═2I-+SO42-+4H+ | |
| C. | 硝酸银溶液中滴加过量氨水:Ag++NH3•H2O═AgOH↓+NH4+ | |
| D. | 0.5 mol/L NaHSO4与0.5 mol/L Ba(OH)2混合至溶液呈中性:Ba2++OH-+SO42-+H+═BaSO4↓+H2O |
分析 A.离子方程式两边正电荷不相等,违反了电荷守恒;
B.碘单质能够将二氧化硫氧化成硫酸;
C.氨水过量,反应生成银氨络离子,不会生成沉淀;
D.溶液呈中性时,硫酸氢钠与氢氧化钡的物质的量之比为2:1.
解答 解:A.用氯化铁溶液腐蚀铜板,反应生成了氯化亚铁和氯化铜,正确的离子方程式为:Cu+2Fe3+═Cu2++2Fe2+,故A错误;
B.碘水中通入适量的SO2,反应生成硫酸和HI,反应的离子方程式为:I2+SO2+2H2O═2I-+SO42-+4H+,故B正确;
C.二者反应生成银氨溶液,先发生反应Ag ++NH3•H2O=AgOH↓+NH4+,后发生反应:AgOH+2NH3•H2O=[Ag(NH3)2]++OH-+2H2O,故C错误;
D.0.5mol/L NaHSO4与0.5 mol/L Ba(OH)2混合至溶液呈中性,正确的离子方程式为:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓,故D错误;
故选B.
点评 本题考查了离子方程式的书写判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式正误判断常用方法,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等)等.

练习册系列答案
 每课必练系列答案
每课必练系列答案
相关题目
17.某固体可能含有NH4+、Cu2+、Na+、Cl-、CO32-、SO42-中的几种离子,取等质量的两份该固体,进行如下实验(不考虑盐类的水解及水的电离);
(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀.
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(保准状况).
下列说法正确的是( )
(1)一份固体溶于水得无色透明溶液,加入足量BaCl2溶液,得沉淀6.63g,在沉淀中加入过量稀盐酸,仍有4.66g沉淀.
(2)另一份固体与过量NaOH固体混合后充分加热,产生使湿润的红色石蕊试纸变蓝色的气体0.672L(保准状况).
下列说法正确的是( )
| A. | 该固体中一定含有NH4+、CO32-、SO42-、Na+ | |
| B. | 该固体中一定没有Cu2+、Cl-、Na+ | |
| C. | 该固体中只含有NH4+、CO32-、SO42-、Cl- | |
| D. | 根据以上实验,无法确定该固体中有Na+ |
14.葛根素具有降血压等作用,其结构简式如图,下列有关说法正确的是( )
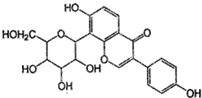

| A. | 该物质在一定条件下能发生消去反应、加成反应、取代反应 | |
| B. | 葛根素的分子式为C21H22O9 | |
| C. | 一定条件下1mol 该物质与浓溴水反应最多能消耗3mol Br2 | |
| D. | 一定条件下1mol 该物质与H2反应最多能消耗7mol H2 |
1.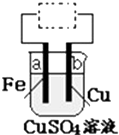 用铁片(电极a)、铜片(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )
用铁片(电极a)、铜片(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )
 用铁片(电极a)、铜片(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )
用铁片(电极a)、铜片(电极b)和CuSO4溶液可以构成原电池或电解池,如图所示.则下列说法正确的是( )| A. | 构成原电池时b极反应为:Cu-2e-═Cu2+ | |
| B. | 构成的原电池或电解池工作后就可能产生大量气体 | |
| C. | 构成电解池时b 极质量既可能减少也可能增加 | |
| D. | 构成电解池时a极质量一定会减少 |
11.以下指定反应的离子方程式正确的是( )
| A. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液至SO42-恰好沉淀完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O | |
| B. | 向苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |
| C. | 氧化亚铁溶于稀硝酸:3FeO+8H++NO3-═3Fe3++NO↑+4H2O | |
| D. | 将0.4 mol•L-1的NaAlO2溶液和0.7 mol•L-1的盐酸等体积混合:4AlO${\;}_{2}^{-}$+7H++H2O═3Al(OH)3↓+Al3+ |
18.X、Y、Z、W是原子序数依次增大的四种短周期元素.Y和Z位于同一周期,可组成中学常见的共价化合物YZ和YZZ,X和Z的原子最外层电子数之和等于W的原子最外层电子数,25℃时0.01mol/L X和W形成化合物的水溶液pH为2.下列说法正确的是( )
| A. | Y元素含氧酸的酸性比W的弱 | |
| B. | Z和W在自然界均能以游离态存在 | |
| C. | YZ和YZ2均可以被NaOH溶液吸收 | |
| D. | X和Y能形成既含极性键又含非极性键的分子 |
15.分子式为C4H8O2且能与氢氧化钠溶液反应的有机物(不考虑立体异构和醛类物质)有( )
| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
16.NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 6.0gSiO2晶体中存在的共价键总数为2 NA | |
| B. | 1L 0.1mol•L-1的Na2CO3溶液中含有阳离子的总数为2NA | |
| C. | 标准状况下,2.0gD2O中含有的质子数和中子数均为NA个 | |
| D. | 室温时,pH=12的Ba(OH)2溶液中,氢氧根离子数目为10-2N |