题目内容
13.玻璃棒是化学实验中最常用的一种仪器.下列实验中要用到玻璃棒的是( )| A. | 用pH试纸测定水样的pH | B. | 检验硫酸根离子 | ||
| C. | 实验室用高锰酸钾制取氧气 | D. | 从碘水中萃取碘 |
分析 A.玻璃棒蘸取水样滴在pH试纸上;
B.选择盐酸、氯化钡在试管中检验硫酸根离子;
C.利用固体加热装置制取氧气;
D.利用萃取、分液、蒸馏从碘水中萃取碘.
解答 解:A.玻璃棒蘸取水样滴在pH试纸上,测定水样的pH,则该实验需要玻璃棒,故A选;
B.选择盐酸、氯化钡在试管中检验硫酸根离子,利用试管、胶头滴管等可检验,该实验不需要玻璃棒,故B不选;
C.利用固体加热装置制取氧气,需要试管、酒精灯、集气瓶等,不需要玻璃棒,故C不选;
D.利用萃取、分液、蒸馏从碘水中萃取碘,需要分液漏斗、烧杯、蒸馏烧瓶、锥形瓶等,不需要玻璃棒,故D不选;
故选A.
点评 本题考查化学实验方案的评价,为高频考点,把握仪器的使用、离子检验、气体的制备、混合物分离、实验操作为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
4.25℃时,pH=3的盐酸中由水电离出的H+离子浓度是pH=5的盐酸中由水电离的H+离子浓度的多少倍( )
| A. | 10-2 | B. | 102 | C. | 2 | D. | 12 |
1.乙酸与乙醇的酯化反应中,乙醇的结构简式为 C2H518OH,则反应一段时间后,18O原子存在于( )
| A. | 存在于乙酸的分子中 | B. | 存在于乙醇的分子中 | ||
| C. | 存在于乙酸和乙酸乙酯分子中 | D. | 存在于乙醇和乙酸乙酯分子中 |
8.NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 1.0L0.1 mol/•LNa2S溶液中含有的S2-离子数为0.1NA | |
| B. | 一定条件下,4.6g的Na完全与O2反应生成7.2g产物时失去的电子数为0.2NA | |
| C. | 通过化学变化可以实现16O与18O间的相互转化 | |
| D. | 电镀铜时,若阴极得到电子数为2NA,则阳极质量减少不一定等于64g |
18.下列有关说法正确的是( )
| A. | 将pH=10的浓氨水稀释,溶液中所有离子的浓度都减小 | |
| B. | CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,反应速率V(H2)和氢气的平衡转化率均增大 | |
| D. | pH=3的盐酸和pH=11的氨水等体积混合液中,c(H+)<c(OH-) |
2.下列叙述正确的是( )
| A. | 1.00molNaCl中含有6.02×1023个NaCl分子 | |
| B. | 从100mL,1 mol/L的NaCl溶液中取出10 mL,其物质的量浓度是0.1 mol/L | |
| C. | 1.00mol NaCl中,所有Na+的最外层电子总数为8×6.02×1023 | |
| D. | 欲配制1.00L,1.00mol•L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 |
3.下列反应中,属于取代反应的是( )
| A. | 在催化剂存在条件下乙烯与溴反应制 1,2-二溴乙烷 | |
| B. | 在一定条件下苯与氢气反应制取环己烷 | |
| C. | 甲苯使酸性高锰酸钾溶液褪色 | |
| D. | 苯与浓硝酸、浓硫酸混合共热制取硝基苯 |
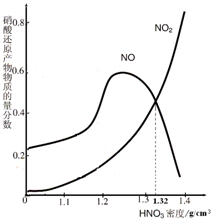 绿矾受热分解后的产物为不含硫元素的固体A、SO2、SO3和H2O.回答下列问题:
绿矾受热分解后的产物为不含硫元素的固体A、SO2、SO3和H2O.回答下列问题: