��Ŀ����
19����ΪԪ�����ڱ���һ����| ̼ | �� | Y | |
| X | �� | Z |
��1��YԪ�������ڱ��е�λ��Ϊ�ڶ����ڵڢ�IA�壮
��2������Ԫ��ԭ�Ӱ뾶�����ǣ�дԪ�ط��ţ�Si��
��3��������ʵ����˵��Z Ԫ�صķǽ����Ա�S Ԫ�صķǽ�����ǿ���ǣ�b
a��Z�ĵ�����H2S��Һ��Ӧ����Һ�����
b��Z�ĺ�����HZO3���Ա�H2SO4ǿ
c��Z��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸ�
d��������SZ2��S�����ۣ�Z�Ը���
��4������ijԪ�ص���ۺ�����������̬�⻯�ﷴӦ����һ���Σ�����������ѧ��������Ϊ���Ӽ������ۼ���
��5��̼��Y��������Ԫ�ذ�1��l��l�������γɻ����ÿ��ԭ�Ӷ��ﵽ8���ӵ��ȶ��ṹ���û�����ĵ���ʽΪ
 ��
����6��ͭ��һ��Ũ�ȵ����������Ļ���ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���������ж����壬���ɱ�������Ԫ����ɣ��������Է���������С��50��Ϊ��ֹ��Ⱦ����������������ȫת��Ϊ��ۺ������Σ�����1L 2.2mol/LNaOH��Һ��lmolO2������������ķ���ʽ�����ʵ����ֱ�ΪNO 0.9mol��NO2 1.3mol����������ͭ���ʵ���Ϊ2mol��
���� ��Ԫ����Ԫ�����ڱ������λ�ã���֪XΪSiԪ�أ�YΪOԪ�أ�ZΪClԪ�أ�
��1������Ԫ��������=���Ӳ���������������=������������
��2��ͬ���ڴ�������ԭ�Ӱ뾶��С��ͬ������ϵ���ԭ�Ӱ뾶������
��3��������ۺ����������ǿ�����⻯���ȶ��Ի��뵥����������Ӧ���׳̶ȡ����ʵ�������ǿ������������Ԫ�صĻ��ϼ۵��ж�Ԫ�طǽ�����ǿ����
��4������ijԪ�ص���ۺ�����������̬�⻯�ﷴӦ����һ���Σ�����ΪNH4NO3��
��5��̼������������Ԫ�ذ�1��l��l�������γɻ����ÿ��ԭ�Ӷ��ﵽ8���ӵ��ȶ��ṹ���û�������Cԭ����Oԭ�ӡ�Sԭ��֮��ֱ��γ�2�Թ��õ��Ӷԣ�
��6��ͭ��һ��Ũ�ȵ����������Ļ���ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���������ж�����ΪNO��NO2������ת��ΪNaNO3�����NO��NO2�����ʵ���������ԭ���غ㡢�����غ���ʽ������Ե����ʵ��������ݵ����غ�ɼ�����������ͭ�����ʵ�����
��� �⣺��Ԫ����Ԫ�����ڱ������λ�ã���֪XΪSiԪ�أ�YΪOԪ�أ�ZΪClԪ�أ�
��1��YΪOԪ�أ�ԭ�Ӻ�����2�����Ӳ㣬����������Ϊ6��λ�����ڱ��еڶ����ڵڢ�IA�壬
�ʴ�Ϊ���ڶ����ڵڢ�IA�壻
��2��ͬ���ڴ�������ԭ�Ӱ뾶��С��ͬ������ϵ���ԭ�Ӱ뾶��������ԭ�Ӱ뾶����ΪSi��
�ʴ�Ϊ��Si��
��3��a��������H2S��Һ��Ӧ����Һ����ǣ�˵�������������Ա���ǿ����˵��ClԪ�صķǽ����Ա�SԪ�صķǽ�����ǿ����a��ȷ��
b��Ӧ������ۺ�����HClO4���Ա�H2SO4ǿ�ж�ClԪ�طǽ����Ա����ǿ����b����
c��Ԫ�صķǽ�����Խǿ���⻯����ȶ���Խǿ��Y��S��Ԫ�صļ��⻯�����ȷֽ⣬ǰ�ߵķֽ��¶ȸߣ�˵��Y�ķǽ����Խ�ǿ����c��ȷ��
d��������SCl2��S�����ۣ�Cl�Ը��ۣ�˵��Cl�Լ��ϵ���������ǿ��˵��ClԪ�طǽ����Ը�ǿ����d��ȷ��
�ʴ�Ϊ��b��
��4������ijԪ�ص���ۺ�����������̬�⻯�ﷴӦ����һ���Σ�����ΪNH4NO3���������Ӽ������ۼ���
�ʴ�Ϊ�����Ӽ������ۼ���
��5��̼������������Ԫ�ذ�1��l��l�������γɻ����ÿ��ԭ�Ӷ��ﵽ8���ӵ��ȶ��ṹ���û�����ΪCOS����������Cԭ����Oԭ�ӡ�Sԭ��֮��ֱ��γ�2�Թ��õ��Ӷԣ�����ʽΪ ��
��
�ʴ�Ϊ�� ��
��
��6��ͭ��һ��Ũ�ȵ����������Ļ���ᷴӦ�����ɵ���ֻ������ͭ��ͬʱ���������ж�����ΪNO��NO2������ת��ΪNaNO3��1mol�������뷴Ӧת�Ƶ��ӵ����ʵ���Ϊ4mol�����NO��NO2�����ʵ����ֱ�Ϊxmol��ymol����
$\left\{\begin{array}{l}{x+y=2.2}\\{x+3y=4}\end{array}\right.$
��ã�x=1.3��y=0.9��
���ݵ����غ㣺n��CuSO4��=$\frac{4mol}{2}$=2mol��
�ʴ�Ϊ��NO 0.9mol��NO2 1.3mol��2mol��
���� ���⿼��Ԫ�����ڱ���Ԫ�������ɡ�����ʽ��������ԭ��Ӧ�ļ����֪ʶ�����ս����ԡ��ǽ�����ǿ���ȽϷ�����ע�������غ�˼���ڻ�ѧ�����е�Ӧ�ã�����������ѧ���ķ�����������ѧ����������

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�| A�� | ���ϡ���Ȼ���Ǹ߷��ӻ����� | |
| B�� | ��ϩ������ϩ�ͱ������о�����̼̼˫�� | |
| C�� | ������ë����˿��������Ȼ��ά�� | |
| D�� | ������Ҵ�����Na2CO3��Һ�������� |
| A�� | ��Ҫ���Ȳ��ܷ����ķ�Ӧһ�������ȷ�Ӧ | |
| B�� | ���ȷ�Ӧ�ڳ�����һ���������� | |
| C�� | ���ȷ�Ӧ�����Ȳ����ܽ��з�Ӧ | |
| D�� | ��Ӧ�����Ȼ��Ƿ������ɷ�Ӧ��������������е�����������Դ�С�������� |
| A�� | ������ܶȲ��ٱ仯 | B�� | NH3�� NO �ķ�Ӧ������� | ||
| C�� | ��Ӧ���ʲ��ٱ仯 | D�� | NO ��H2O Ũ�ȱȲ��ٱ仯 |
| A�� | 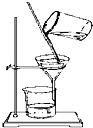 | B�� | 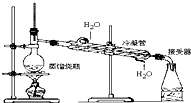 | ||
| C�� |  | D�� | 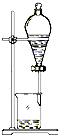 |
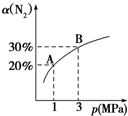 ij�¶��£����ڷ�ӦN2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol��N2��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������
ij�¶��£����ڷ�ӦN2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol��N2��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ��ͼ��ʾ������˵����ȷ���ǣ�������| A�� | ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K��A��=K��B�� | |
| B�� | ��1 mol������3 mol����������1 L�ܱ������з�����Ӧ���ų�������Ϊ92.4 kJ | |
| C�� | �����¶ȣ��淴Ӧ������������Ӧ���ʼ�С | |
| D�� | ������Ӧ�ﵽƽ�������H2Ũ�ȣ�ƽ�������ƶ���H2ת�������� |
| A�� | NH4HCO3���ڹ�����NaOH��Һ�У�HCO3-+OH-=CO32-+H2O | |
| B�� | �����������Ʒ�����ˮ�У�Na+2H2O�TNa++2OH-+H2�� | |
| C�� | FeCl3��Һ��Cu�ķ�Ӧ��Cu+Fe3+=Cu2++Fe2+ | |
| D�� | FeSO4��Һ�м���H2O2��2Fe2++H2O2+2H+=2Fe3++2H2O |
 ��1����֪����C��s��+O2��g��=CO2��g����H=a kJ•mol-1
��1����֪����C��s��+O2��g��=CO2��g����H=a kJ•mol-1��2CO��g��+O2��g��=2CO2��g����H=b kJ•mol-1��
��TiO2��s��+2Cl2��g��=TiCl4��s��+O2��g����H=c kJ•mol-1��
��TiO2��s��+2Cl2��g��+2C��s��=TiCl4��s��+2CO��g���ġ�H=c+2a-bkJ•mol-1�����ú�a��b��c��ʽ�ӱ�ʾ��
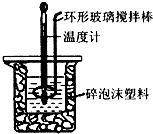
��2����50mL 0.50mol•L-1������50mL 0.55mol•L-1 NaOH��Һ������ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺
| ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | �¶Ȳ� ��t2-t1��/�� | |||
| ƽ��ֵ | |||||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.2 | 24.45 | 27.6 | 3.15 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
��װ���д�С�ձ�֮����������ĭ���ϵ�Ŀ���Ǽ���ʵ������е�������ʧ��
��ijͬѧʵ���¼���������ϱ���ʾ�����м�¼����ֹ�¶���ָ�����Һ������¶ȣ�
�ܼ����ʵ�鷢���кͷ�Ӧʱ�ų�������Ϊ1344J[�кͺ����ɵ���Һ�ı�����c=4.2J•��g•�棩-1��ϡ��Һ���ܶȶ�Ϊ1g•cm-3]��
������50mL 0.55mol•L-1�İ�ˮ��NH3•H2O������NaOH��Һ��������ʵ�飬ͨ����õķ�Ӧ���������к��ȣ���õ��к��ȡ�H��ƫ���ƫ����ƫ���䡱����ԭ����һˮ�ϰ�Ϊ������ʣ���Ӧ�����е�����Ҫ�����������ʷų�������ƫ�٣���Hƫ��
| A�� | ���ý����ƻ��߽����� | B�� | �������� | ||
| C�� | ���ú������ | D�� | ���ú˴Ź������� |