题目内容
10.下列说法中正确的是( )| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | 放热反应在常温下一定很容易发生 | |
| C. | 吸热反应不加热不可能进行反应 | |
| D. | 反应是吸热还是放热是由反应物和生成物所具有的总能量的相对大小而决定的 |
分析 A..需要加热才能进行的化学反应不一定是吸热反应;
B.放热反应在常温下不一定很容易发生,吸热反应在常温下不一定不能发生;
C.吸热反应常温下也可以发生反应;
D.反应是吸热还是放热是由反应物和生成物所具有的总能量的相对大小而决定的,若反应物总能量大于生成物总能量为放热反应,反应物总能量小于生成物总能量为吸热反应.
解答 解:A.需要加热才能进行的化学反应不一定是吸热反应,如铝热反应,需要加热,但属于放热反应,故A错误;
B.放热反应在常温下不一定很容易发生,如碳与氧气的反应为放热反应,但须点燃,故B错误;
C.有些吸热反应在常温下可自发进行,如氯化铵和氢氧化钡的反应,故C错误;
D.反应是吸热还是放热是由反应物和生成物所具有的总能量的相对大小而决定的,若反应物总能量大于生成物总能量为放热反应,反应物总能量小于生成物总能量为吸热反应,故D正确;
故选D.
点评 本题考查了反应热类型的判断,要注意反应热与反应条件无关,和反应物和生成物的总能量有关,掌握基础是解题关键,题目难度不大.

练习册系列答案
相关题目
1.列有关化学用语表达不正确的是( )
| A. | 氨气分子的电子式: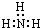 | B. | CS2分子的结构式:S═C═S | ||
| C. | S2-的结构示意图: | D. | CH4的分子模型示意图为: |
18.某固体混合物可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的两种或多种组成,现对该混合物做如下实验,所得现象和有关数据如图所示(气体体积数据已换算成标准状况下的体积),关于该固体混合物,下列说法不正确的是( )


| A. | 一定含有Al,其质量为2.7g | |
| B. | 一定不含有FeCl2,含有少量AlCl3 | |
| C. | 混合物中含有0.05molMgCl2 | |
| D. | 一定含有(NH4)2SO4和MgCl2,且物质的量相等 |
15.某同学根据外界条件对化学反应速率的影响原理,设计了硫代硫酸钠与硫酸反应有关实验,
实验过程的数据记录如下表,请结合表中信息,回答有关问题:
(1)写出上述反应的离子方程式S2O32-+2H+═S↓+SO2↑+H2O.
(2)①能说明温度对该反应速率影响的组合比较是BD;(填实验序号)
②A和B、A和C的组合比较所研究的问题是相同温度条件下浓度对该反应速率的影响.
(3)教材是利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小的可能原因:SO2可溶于水,测定不精确或实验装置较复杂,不易控制.
实验过程的数据记录如下表,请结合表中信息,回答有关问题:
| 实验序号 | 反应温度(℃) | 参加反应的物质 | ||||
| Na2S2O3 | H2SO4 | H2O | ||||
| V/mL | c/mol•L-1 | V/mL | c/mol•L-1 | V/mL | ||
| A | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
| B | 20 | 5 | 0.1 | 10 | 0.1 | 5 |
| C | 20 | 10 | 0.1 | 5 | 0.1 | 5 |
| D | 40 | 5 | 0.1 | 10 | 0.1 | 5 |
(2)①能说明温度对该反应速率影响的组合比较是BD;(填实验序号)
②A和B、A和C的组合比较所研究的问题是相同温度条件下浓度对该反应速率的影响.
(3)教材是利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小的可能原因:SO2可溶于水,测定不精确或实验装置较复杂,不易控制.
2.如表为元素周期表短周期的一部分,请用化学用语(元素符号或化学式)回答相关问题:
(1)⑥元素在周期表中的位置为第三周期第ⅢA族.
(2)表中序号元素中半径最大的常见离子是S2-.
(3)表中最高价氧化物对应水化物的碱性最强的物质的电子式为 ,酸性最强的物质的化学式是HClO4,气态氢化物最稳定的物质的化学式是HF.
,酸性最强的物质的化学式是HClO4,气态氢化物最稳定的物质的化学式是HF.
(4)元素非金属性强弱比较有很多方法,其中③和⑧的非金属性强弱的探究方案中不可行的是A(填序号)
A.比较两种氢化物的熔沸点高低 B.比较氢化物的稳定性
C.通过和铁反应,比较得电子能力 D.通过置换反应
(5)由①和②两种元素组成的化合物,同条件下与氧气密度相当,请写出该分子的电子式 .
.
(6)⑦与⑨两元素的单质反应生成1mol⑦的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式Si(s)+2Cl2(g)=SiCl4(l)△H=-687kJ/mol.
| ① | |||||||
| ② | ③ | ④ | |||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)表中序号元素中半径最大的常见离子是S2-.
(3)表中最高价氧化物对应水化物的碱性最强的物质的电子式为
 ,酸性最强的物质的化学式是HClO4,气态氢化物最稳定的物质的化学式是HF.
,酸性最强的物质的化学式是HClO4,气态氢化物最稳定的物质的化学式是HF.(4)元素非金属性强弱比较有很多方法,其中③和⑧的非金属性强弱的探究方案中不可行的是A(填序号)
A.比较两种氢化物的熔沸点高低 B.比较氢化物的稳定性
C.通过和铁反应,比较得电子能力 D.通过置换反应
(5)由①和②两种元素组成的化合物,同条件下与氧气密度相当,请写出该分子的电子式
 .
.(6)⑦与⑨两元素的单质反应生成1mol⑦的最高价化合物,恢复至室温,放热687kJ,已知该化合物的熔、沸点分别为-69℃和58℃,写出该反应的热化学方程式Si(s)+2Cl2(g)=SiCl4(l)△H=-687kJ/mol.
19.表为元素周期表的一部分
回答下列问题
(1)Y元素在周期表中的位置为第二周期第ⅤIA族.
(2)表中元素原子半径最大的是(写元素符号)Si.
(3)下列事实不能说明Z 元素的非金属性比S 元素的非金属性强的是:b
a.Z的单质与H2S溶液反应,溶液变浑浊
b.Z的含氧酸HZO3酸性比H2SO4强
c.Z和S两元素的简单氢化物受热分解,前者的分解温度高
d.化合物SZ2中S显正价,Z显负价
(4)表中某元素的最高价含氧酸与其气态氢化物反应生成一种盐,该盐所含化学键的类型为离子键、共价键.
(5)碳、Y和硫三种元素按1:l:l个数比形成化合物,每个原子都达到8电子的稳定结构,该化合物的电子式为 .
.
(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成两种有毒气体,均由表中两种元素组成,气体的相对分子质量都小于50.为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/LNaOH溶液和lmolO2,则两种气体的分子式及物质的量分别为NO 0.9mol,NO2 1.3mol,生成硫酸铜物质的量为2mol.
| 碳 | 氮 | Y | |
| X | 硫 | Z |
(1)Y元素在周期表中的位置为第二周期第ⅤIA族.
(2)表中元素原子半径最大的是(写元素符号)Si.
(3)下列事实不能说明Z 元素的非金属性比S 元素的非金属性强的是:b
a.Z的单质与H2S溶液反应,溶液变浑浊
b.Z的含氧酸HZO3酸性比H2SO4强
c.Z和S两元素的简单氢化物受热分解,前者的分解温度高
d.化合物SZ2中S显正价,Z显负价
(4)表中某元素的最高价含氧酸与其气态氢化物反应生成一种盐,该盐所含化学键的类型为离子键、共价键.
(5)碳、Y和硫三种元素按1:l:l个数比形成化合物,每个原子都达到8电子的稳定结构,该化合物的电子式为
 .
.(6)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成两种有毒气体,均由表中两种元素组成,气体的相对分子质量都小于50.为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1L 2.2mol/LNaOH溶液和lmolO2,则两种气体的分子式及物质的量分别为NO 0.9mol,NO2 1.3mol,生成硫酸铜物质的量为2mol.
14.将磷肥生产中形成的副产物石膏( CaSO4•2H2O)转化为硫酸钾肥料和氯化钙水合物储热材料,无论从经济效益、资源综合利用还是从环境保护角度看都县有重要意义.以下是石膏转化为硫酸钾和氯化钙的工艺流程示意图.
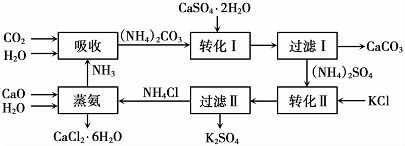
(1)本工艺中所用的原料除CaSO4•2H2O、KCl外,还需要CaCO3(或CaO)、NH3、H2O等原料.
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式CaSO4+CO32-=CaCO3+SO42-
(3)过滤I操作所得固体中,除CaC03外还含有CaSO4(填化学式)等物质,该固体可用作生产水泥的原料.
(4)过滤I操作所得滤液是(NH4)2SO4溶液.检验滤液中含有CO32-的方法是:取少量溶液,滴加稀盐酸,若有气泡产生则还含有CO32-,反之则不含有CO32-
(5)已知不同温度下K2SO4在l00g水中达到饱和时溶解的量如下表:
60℃时K2S04的饱和溶液591g冷却到0℃,可析出K2S04晶体54g.
(6)氯化钙结晶水合物(CaCl2•6H2O)是目前常用的无机储热材料,选择的依据是ad.
a.熔点较低(29℃熔化) b.能导电 c.能制冷 d.无毒
(7)上述工艺流程中体现绿色化学理念的是:碳酸钙用于制水泥原料、硫酸钙和氯化钾转化为硫酸钾和氯化钙、氨在工艺中循环使用(原子利用率高,没有有害物质排放到环境中).

(1)本工艺中所用的原料除CaSO4•2H2O、KCl外,还需要CaCO3(或CaO)、NH3、H2O等原料.
(2)写出石膏悬浊液中加入碳酸铵溶液后发生反应的离子方程式CaSO4+CO32-=CaCO3+SO42-
(3)过滤I操作所得固体中,除CaC03外还含有CaSO4(填化学式)等物质,该固体可用作生产水泥的原料.
(4)过滤I操作所得滤液是(NH4)2SO4溶液.检验滤液中含有CO32-的方法是:取少量溶液,滴加稀盐酸,若有气泡产生则还含有CO32-,反之则不含有CO32-
(5)已知不同温度下K2SO4在l00g水中达到饱和时溶解的量如下表:
| 温度(℃) | 0 | 20 | 60 |
| K2SO4溶解得量(g) | 7.4 | 11.1 | 18.2 |
(6)氯化钙结晶水合物(CaCl2•6H2O)是目前常用的无机储热材料,选择的依据是ad.
a.熔点较低(29℃熔化) b.能导电 c.能制冷 d.无毒
(7)上述工艺流程中体现绿色化学理念的是:碳酸钙用于制水泥原料、硫酸钙和氯化钾转化为硫酸钾和氯化钙、氨在工艺中循环使用(原子利用率高,没有有害物质排放到环境中).
 ;KCl第电子式
;KCl第电子式 .
. ;
;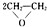 ;
;