籾朕坪否
10⤴和双光怏麗嵎議來嵎乏會⇧音屎鳩議頁↙ ⇄| A⤴ | 圻徨磯抄⦿Na〽Mg〽Al | B⤴ | 犯糧協來⦿HCl﹅HBr﹅HI | ||
| C⤴ | 磨來膿樋⦿H2SiO4〽H2CO3〽H2SO4 | D⤴ | 匪泣⦿SiO2﹅NaCl﹅CO2 |
蛍裂 A⤴揖巓豚貫恣﨑嘔圻徨磯抄受弌◉
B⤴掲署奉來埆膿⇧狽晒麗埆糧協◉
C⤴掲署奉來埆膿⇧恷互勺根剳磨議磨來埆膿◉
D⤴匯違栖傍⇧匪泣葎圻徨唱悶﹅宣徨唱悶﹅蛍徨唱悶⤴
盾基 盾⦿A⤴揖巓豚貫恣﨑嘔圻徨磯抄受弌⇧夸圻徨磯抄⦿Na﹅Mg﹅Al⇧絞A危列◉
B⤴掲署奉來Cl﹅Br﹅I⇧犯糧協來⦿HCl﹅HBr﹅HI⇧絞B屎鳩◉
C⤴掲署奉來S﹅C﹅Si⇧磨來膿樋⦿H2SiO4〽H2CO3〽H2SO4⇧絞C屎鳩◉
D⤴匯違栖傍⇧匪泣葎圻徨唱悶﹅宣徨唱悶﹅蛍徨唱悶⇧夸匪泣⦿SiO2﹅NaCl﹅CO2⇧絞D屎鳩◉
絞僉A⤴
泣得 云籾深臥巓豚燕才巓豚舵⇧葎互撞深泣⇧委燐圷殆議了崔、來嵎、圷殆巓豚舵吉葎盾基議購囚⇧迦嶷蛍裂嚥哘喘嬬薦議深臥⇧廣吭号舵來岑紛議哘喘⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 恬匍絹擬狼双基宛
恬匍絹擬狼双基宛
屢購籾朕
5⤴嬬繍蛍艶根嗤Cu2+、Fe3+、Al3+、Mg2+、Fe2+、NH4+、Na+ 宣徨議鈍嶽卑匣匯肝來授艶蝕栖議編質頁↙ ⇄
| A⤴ | NaHCO3卑匣 | B⤴ | NaOH卑匣 | C⤴ | KSCN卑匣 | D⤴ | 葦邦 |
15⤴葦賑頁伏恢晒景、嵓磨吉議嶷勣圻創⇧律汎栽撹葦繁断序佩阻匯狼双議冩梢⤴
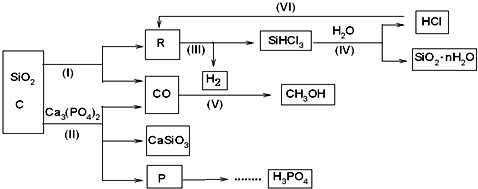
↙1⇄眉紀晒錻邦盾辛伏撹葦賑才麗嵎X⇧X議潤更塀葎 ⤴
⤴
↙2⇄厮岑⦿N2↙g⇄+3H2↙g⇄?2NH3↙g⇄@H=-92.4kJ•mol-1⇧僅叢1mol N《N囚俶勣議嬬楚葎946kJ⤴

↙3⇄械梁和⇧﨑amol•L-1議葦邦紗秘吉悶持bmol•L-1議冦磨⇧詞栽卑匣格嶄來⇧夸乎梁業和葦邦議窮宣峠財械方葎$\frac{b〜1{0}^{-7}}{a-b}$↙喘根a才b議旗方塀燕幣⇄⤴
↙4⇄屢揖梁業和⇧﨑遮、厰、央眉倖否持屢揖議冴否畜液否匂嶄梓孚和双眉嶽圭塀蛍艶誘創⇧窟伏郡哘⦿N2↙g⇄+3H2↙g⇄?2NH3↙g⇄⇧霞誼遮否匂嶄H2議峠財廬晒楕葎40%⤴
〙厰否匂嶄軟兵扮郡哘剃﨑↙野^屎﨑 ̄賜^音 ̄⇄卞強⤴
〖器欺峠財扮⇧遮、厰、央眉倖否匂嶄NH3議悶持蛍方喇寄欺弌議乏會葎央﹅遮=厰⤴
↙5⇄孖蛍艶壓150≧、300≧、500≧扮﨑郡哘匂嶄俊n↙N2⇄⦿n↙H2⇄=1⦿3誘創窟郡哘⦿N2↙g⇄+3H2↙g⇄?2NH3↙g⇄⇧乎郡哘器欺峠財扮⇧悶狼嶄NH3議麗嵎議楚蛍方昧儿膿議延晒爆㞍泌夕侭幣⤴
〙150≧扮窟伏議郡哘辛喘爆㞍m↙野^m ̄、^n ̄賜^l ̄⇄燕幣⤴
〖貧夕嶄A、B、C眉泣議峠財械方K議寄弌購狼頁K↙B⇄=K↙C⇄〽K↙A⇄⤴
〗飛B泣扮c↙NH3⇄=0.6mol•L-1⇧夸緩扮郡哘議晒僥峠財械方K=44.4⤴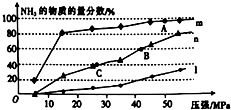
↙1⇄眉紀晒錻邦盾辛伏撹葦賑才麗嵎X⇧X議潤更塀葎
 ⤴
⤴↙2⇄厮岑⦿N2↙g⇄+3H2↙g⇄?2NH3↙g⇄@H=-92.4kJ•mol-1⇧僅叢1mol N《N囚俶勣議嬬楚葎946kJ⤴

↙3⇄械梁和⇧﨑amol•L-1議葦邦紗秘吉悶持bmol•L-1議冦磨⇧詞栽卑匣格嶄來⇧夸乎梁業和葦邦議窮宣峠財械方葎$\frac{b〜1{0}^{-7}}{a-b}$↙喘根a才b議旗方塀燕幣⇄⤴
↙4⇄屢揖梁業和⇧﨑遮、厰、央眉倖否持屢揖議冴否畜液否匂嶄梓孚和双眉嶽圭塀蛍艶誘創⇧窟伏郡哘⦿N2↙g⇄+3H2↙g⇄?2NH3↙g⇄⇧霞誼遮否匂嶄H2議峠財廬晒楕葎40%⤴
| N↙N2⇄/mol | N↙H2⇄/mol | N↙NH3⇄/mol | |
| 遮 | 1 | 3 | 0 |
| 厰 | 0.5 | 1.5 | 1 |
| 央 | 0 | 0 | 4 |
〖器欺峠財扮⇧遮、厰、央眉倖否匂嶄NH3議悶持蛍方喇寄欺弌議乏會葎央﹅遮=厰⤴
↙5⇄孖蛍艶壓150≧、300≧、500≧扮﨑郡哘匂嶄俊n↙N2⇄⦿n↙H2⇄=1⦿3誘創窟郡哘⦿N2↙g⇄+3H2↙g⇄?2NH3↙g⇄⇧乎郡哘器欺峠財扮⇧悶狼嶄NH3議麗嵎議楚蛍方昧儿膿議延晒爆㞍泌夕侭幣⤴
〙150≧扮窟伏議郡哘辛喘爆㞍m↙野^m ̄、^n ̄賜^l ̄⇄燕幣⤴
〖貧夕嶄A、B、C眉泣議峠財械方K議寄弌購狼頁K↙B⇄=K↙C⇄〽K↙A⇄⤴
〗飛B泣扮c↙NH3⇄=0.6mol•L-1⇧夸緩扮郡哘議晒僥峠財械方K=44.4⤴

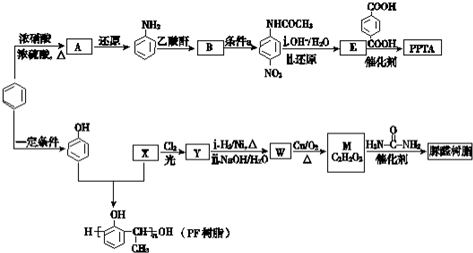
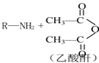 ★R-NHCOCH2+CH2COOH↙R葎癒児⇄
★R-NHCOCH2+CH2COOH↙R葎癒児⇄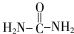 ↙挺殆⇄紀圻徨貧議狽圻徨辛參崧噂罫貧議狽圻徨椎劔嚥遮肌窟伏紗撹郡哘⇧旺抹詔撹互蛍徨⤴
↙挺殆⇄紀圻徨貧議狽圻徨辛參崧噂罫貧議狽圻徨椎劔嚥遮肌窟伏紗撹郡哘⇧旺抹詔撹互蛍徨⤴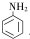 ★B 議郡哘窃侏頁函旗郡哘⤴
★B 議郡哘窃侏頁函旗郡哘⤴ ⤴
⤴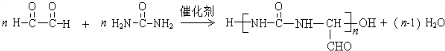 ⤴
⤴ ⤴
⤴