题目内容
15.下列关于同温同压下的两种气体12C18O和14N2的判断正确的是( )| A. | 体积相等时具有的质量相等 | B. | 分子数相等时具有的中子数相等 | ||
| C. | 质量相等时具有的质子数相等 | D. | 体积相等时具有的原子数相等 |
分析 同温同压下,气体的Vm相等,等体积时,根据n=$\frac{V}{{V}_{m}}$可知气体的物质的量相等,结合原子的构成以及相关物理量的计算公式解答该题.
解答 解:A.由于12C18O和14N2的相对分子质量不等,故体积相等的两种气体的质量不等,故A错误;
B.1个12C18O分子中有16个中子,1个14N2分子中含有14个中子,分子数相等但中子数不等,故B错误;
C.12C18O和14N2分子内均有14个质子,由于二者的相对分子质量不等,故等质量的两种分子所具有的质子数不等,故C错误.
D.12C18O和14N2均为双原子分子,同温同压下,体积相等则分子数相等,所具有的原子数相等,故D正确;
故选D.
点评 本题考查基本概念和基本理论知识,意在考查考生对一些重要概念与理论的理解能力,主要是阿伏伽德罗定律及其推论的分析判断,题目难度中等.

练习册系列答案
 赢在课堂名师课时计划系列答案
赢在课堂名师课时计划系列答案
相关题目
20.欲使Ag2CO3(Ksp=8.3×10-12)转化为Ag2C2O4(Ksp=5.3×10-12),必须使( )
| A. | c(C2O42-)<0.64c(CO32-) | B. | c(CO32-)>1.56c(C2O42-) | ||
| C. | c(C2O42-)<1.56c(CO32-) | D. | c(C2O42-)>0.64c(CO32-) |
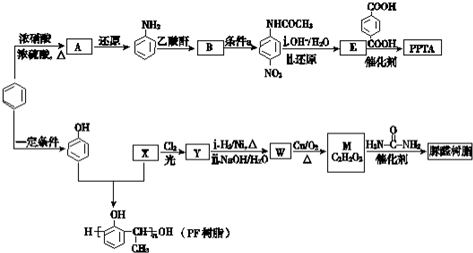
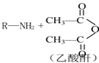 →R-NHCOCH2+CH2COOH(R为烃基)
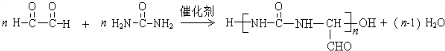
→R-NHCOCH2+CH2COOH(R为烃基)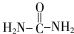 (尿素)氮原子上的氢原子可以像苯酚上的氢原子那样与甲醛发生加成反应,并缩聚成高分子.
(尿素)氮原子上的氢原子可以像苯酚上的氢原子那样与甲醛发生加成反应,并缩聚成高分子.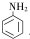 →B 的反应类型是取代反应.
→B 的反应类型是取代反应. .
. .
.