题目内容
18.已知下列热化学方程式:(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
(3)H2(g)+1/2O2(g)═H2O(l)△H3=-285.8kJ/mol
则反应2C(s)+2H2(g)+O2(g)═CH3COOH(l)的焓变为( )
| A. | -488.3 kJ/mol | B. | -244.15 kJ/mol | C. | 488.3 kJ/mol | D. | 244.15 kJ/mol |
分析 根据盖斯定律,2(2)+(3)-(1)可得目标热化学方程式2C(s)+2H2(g)+O2(g)═CH3COOH(l)△H=2△H2+△H3-△H1,据此可计算出该反应的焓变.
解答 解:已知:(1)CH3COOH(l)+2O2(g)═2CO2(g)+2H2O(l)△H1=-870.3kJ/mol
(2)C(s)+O2(g)═CO2(g)△H2=-393.5kJ/mol
(3)2H2(g)+O2(g)═2H2O(l)△H3=-571.6kJ/mol,
根据盖斯定律2(2)+(3)-(1)可得反应2C(s)+2H2(g)+O2(g)═CH3COOH(l),则△H=2△H2+△H3-△H1=870.3kJ/mol+2×(-393.5kJ/mol)+(-571.6kJ/mol)=-488.3 kJ/mol,
故选A.
点评 本题考查利用盖斯定律计算反应热,题目难度不大,明确盖斯定律的内容为解答关键,注意掌握热化学方程式的书写原则,试题培养了学生的灵活应用能力.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案
相关题目
8.“碘钟”实验中,3I-+S2O82-═I3-+2SO42-的反应速率可以用I3-与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大.某探究性学习小组在20℃下进行实验,得到 的数据如下表:
回答下列问题:
(1)该实验的目的是研究反应物I-与S2O82-的浓度对反应速率的影响.
(2)显色时间t1=29.3s.
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为A(填字母).
A.<22.0s B.22.0~44.0sC.>44.0s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是反应速率与反应物起始浓度乘积成正比或显色时间与反应物起始浓度乘积成反比.
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| c(I-)/mol•L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| c(S2O82-)/mol•L-1 | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
(1)该实验的目的是研究反应物I-与S2O82-的浓度对反应速率的影响.
(2)显色时间t1=29.3s.
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为A(填字母).
A.<22.0s B.22.0~44.0sC.>44.0s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是反应速率与反应物起始浓度乘积成正比或显色时间与反应物起始浓度乘积成反比.
9.如表所示是元素周期表示意图的一部分,根据表中10种元素,用元素符号或化学式填空.
(1)①~⑩元素中,金属性最强的是K(填元素符号,下同);化学性质最不活泼是Ar.
(2)①~⑩元素中,最高价氧化物对应的水化物呈两性的元素是Al(填元素符号),该水化物与NaOH溶液反应的离子方程式为Al (OH)3+OH-=AlO2-+2H2O.
(3)①~⑩元素中,最高价氧化物对应的水化物的酸性最强的元素是Cl(填元素符号,下同),碱性最强的元素是K.
(4)⑤、⑥、⑧、⑨所形成的简单离子的半径由大到小的顺序是S2->Cl->K+>Ca2+.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅤⅠA | ⅤⅡA | O |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | |||
| 四 | ⑧ | ⑨ | ⑩ |
(2)①~⑩元素中,最高价氧化物对应的水化物呈两性的元素是Al(填元素符号),该水化物与NaOH溶液反应的离子方程式为Al (OH)3+OH-=AlO2-+2H2O.
(3)①~⑩元素中,最高价氧化物对应的水化物的酸性最强的元素是Cl(填元素符号,下同),碱性最强的元素是K.
(4)⑤、⑥、⑧、⑨所形成的简单离子的半径由大到小的顺序是S2->Cl->K+>Ca2+.
6.根据有机化合物的系统命名法,下列命名正确的是( )
| A. | 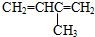 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | B. |  2-羟基丁烷 2-羟基丁烷 | ||
| C. |  2-乙基丁烷 2-乙基丁烷 | D. |  邻羟基苯甲酸 邻羟基苯甲酸 |
13.下列说法正确的是( )
| A. | 最外层有4个电子的原子都是非金属原子 | |
| B. | 同一主族的两种元素的原子序数之差不可能是44 | |
| C. | COCl2分子和CCl4分子中所有原子都满足最外层8电子结构 | |
| D. | 同主族金属的原子,半径越大,熔点越高 |
3.常见元素A、B、C、D、E的原子序数依次增大,其相关信息如表:
(1)E位于元素周期表的位置是第4周期第VIII族.
(2)C元素基态原子的电子排布图 .
.
(3)C单质分子的电子式为 ,C的氢化物在同族元素中氢化物的沸点出现反常,其原因是NH3分子间易形成氢键.
,C的氢化物在同族元素中氢化物的沸点出现反常,其原因是NH3分子间易形成氢键.
(4)D的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为8HCl+KClO4$\frac{\underline{\;\;△\;\;}}{\;}$KCl+4Cl2↑+4H2O.
(5)由A、B两种元素组成的非极性分子有多种,其中乙是一个含4个原子的分子,乙分子的中心原子的杂化方式为sp杂化.已知13g乙完全燃烧放出的热量为600kj,则乙燃烧热的热化学反应方程式是C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(l)△H=-1200kJ/mol.
| 元素 | 相关信息 |
| A | 该元素的一种核素无中子 |
| B | 基态原子核外只有三个能级,且各能级电子数相等 |
| C | 基态原子最外层电子数是其内层电子总数的2.5倍 |
| D | 一个D-离子含18个电子 |
| E | +3价离子3d能级为半充满 |
(2)C元素基态原子的电子排布图
 .
.(3)C单质分子的电子式为
 ,C的氢化物在同族元素中氢化物的沸点出现反常,其原因是NH3分子间易形成氢键.
,C的氢化物在同族元素中氢化物的沸点出现反常,其原因是NH3分子间易形成氢键.(4)D的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为8HCl+KClO4$\frac{\underline{\;\;△\;\;}}{\;}$KCl+4Cl2↑+4H2O.
(5)由A、B两种元素组成的非极性分子有多种,其中乙是一个含4个原子的分子,乙分子的中心原子的杂化方式为sp杂化.已知13g乙完全燃烧放出的热量为600kj,则乙燃烧热的热化学反应方程式是C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(l)△H=-1200kJ/mol.
10.胶状液氢(主要成分是H2和CH4)有望用于未来的运载火箭和空间运输系统.实验测得:101kPa时,H2的燃烧热为285.8kJ•mol-1,CH4的燃烧热为890.3kJ•mol-1.下列热化学方程式书写正确的是( )
| A. | CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ•mol-1 | |
| B. | $\frac{1}{2}$CH4(g)+O2(g)═$\frac{1}{2}$CO2(g)+H2O(l)△H=-445.15 kJ•mol-1 | |
| C. | CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3 kJ | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 |
7.设阿伏加德罗常数(NA)的数值为nA,下列说法不正确的是( )
| A. | 1mol Cl2与足量Fe反应,转移的电子数为2nA | |
| B. | 19.2g纯铜理论上可以制得纯净的硝酸铜的物质的量为0.3NA | |
| C. | 1.8 gAl与足量的盐酸反应放出的氢气为0.1NA | |
| D. | 0.10mol Fe粉与足量水蒸气反应生成的H2分子数为0.10nA |
8.化学与人类的生活、生产息息相关,下列叙述正确的是( )
| A. | “春蚕到死丝方尽、蜡炬成灰泪始干”中的“丝”的主要成分是纤维素,属于天然高分子化合物 | |
| B. | “千锤万凿出深山,烈火焚烧若等闲”的过程中不但有物理变化,也有化学变化 | |
| C. | 日常生活中常用汽油去除衣物上的油污,用热的纯碱溶液洗涤炊具上的油污,两者的原理完全相同 | |
| D. | “84”消毒液的有效成分为NaClO,“洁厕灵”的有效成分为HCl,若将两者混合使用,其杀菌效果和去除厕所污渍的效果都将加强 |