题目内容
11.如图在试管甲中先加入2ml 95%的乙醇,并在摇动下缓慢加入2ml浓硫酸,充分摇匀,冷却后再加入2g无水乙酸(CH3COOH).将试管甲固定在铁架台上,在试管乙中加入5ml饱和碳酸钠溶液,按如图连接好装置进行实验,当试管乙中有明显现象时停止实验.试回答:写出试管甲中发生反应的化学方程式:CH3COOH+C2H5OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O.该实验中球形管丙的作用是防止倒吸.
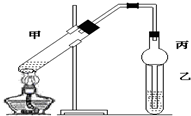
分析 甲中乙酸、乙醇在浓硫酸作用下发生酯化反应生成乙酸乙酯和水,丙中球形结构可防止液体倒吸,以此来解答.
解答 解:试管甲中乙酸、乙醇在浓硫酸作用下发生酯化反应生成乙酸乙酯和水,发生反应的化学方程式为CH3COOH+C2H5OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O.乙醇、乙酸易溶于水,则该实验中球形管丙的作用是防止倒吸,
故答案为:CH3COOH+C2H5OH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O;防止倒吸.
点评 本题考查有机物的结构与性质,为高频考点,把握乙酸和乙醇的性质、有机反应为解答的关键,侧重分析与应用能力的考查,注意球形管的作用,题目难度不大.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
13.下列说法正确的是( )
| A. | 电子从3s能级跃迁到3p能级形成的光谱是发射光谱 | |
| B. | 白磷(P4)分子是正四面体结构,故分子中的键角为109°28′ | |
| C. | NO2- 中心原子采取sp2杂化,分子空间构型为“V”形 | |
| D. | 原子晶体熔点不一定比金属晶体高,分子晶体熔点不一定比金属晶体低 |
20.粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,除去这些杂质的试剂可选用①Na2CO3、②NaOH、③BaCl2、④HCl,加入的先后顺序可以是( )
| A. | ①②③④ | B. | ②③①④ | C. | ②①③④ | D. | ③②④① |
1.9.6g碳与一定量的氧气在密闭容器中于高温下充分反应后,测得相同条件下的压强是反应前的1.6倍,则原氧气的质量为( )
| A. | 8g | B. | 16g | C. | 24g | D. | 32g |
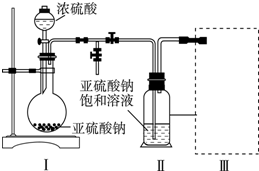
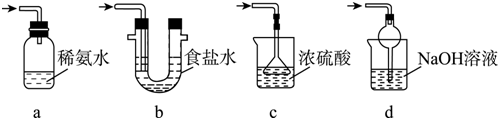
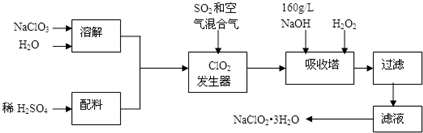
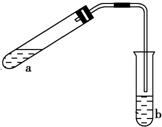 可用如图所示的装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空:
可用如图所示的装置制取少量乙酸乙酯(酒精灯等在图中均已略去).请填空: A是石油裂解主要产物之一,其产量常用于衡量一个石油化工发展水平的标志.
A是石油裂解主要产物之一,其产量常用于衡量一个石油化工发展水平的标志.