题目内容
8.用二氧化锰和浓盐酸反应制取氯气,当有4mol氯化氢被氧化时,生成的氯气在标况下的体积是44.8L.分析 据4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O此方程式得,参加反应的HCl4mol,被氧化的HCl2mol,据此进行计算,
解答 解:据4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O此方程式得,参加反应的HCl4mol,被氧化的HCl2mol,
4HCl(浓)+MnO2$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O~被氧化2HCl
22.4 2
44.8 4
则:V(Cl2)=44.8L,
故答案为:44.8.
点评 明确参加反应的盐酸与被氧化的盐酸之间关系以及正确书写方程式是本题解题的关键,本题难度中等.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
18.下列物质性质变化规律正确的是( )
| A. | HI、HBr、HCl、HF的沸点依次降低 | B. | O、F、H的原子半径依次减小 | ||
| C. | 干冰、钠、冰的熔点依次降低 | D. | 金属Na、Mg、Al的硬度依次降低 |
19.下列关于价电子排布为3s23p4的原子描述正确的是( )
| A. | 它的元素符号为O | |
| B. | 它的核外电子排布式为1s22s22p63s23p4 | |
| C. | 可以与H2化合生成液态化合物 | |
| D. | 其电子排布图为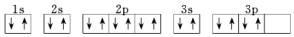 |
3.下列各组离子在溶液中能大量共存的是( )
| A. | Fe3+、Cl-、NO3- | B. | K+、HCO3-、OH- | C. | Na+、HCO3-、H+ | D. | NH4+、H+、SO32- |
9.下列表示对应化学反应的离子方程式正确的是( )
| A. | 向碳酸氢钙溶液中加入少量烧碱溶液:Ca2++2HCO3-+20H-═CaCO3↓+CO32-+H2O | |
| B. | 碘水中通入足量的 S02:I2+SO2+2H2O═2I-+S042-+4H+ | |
| C. | 向氯化铝溶液中滴加过量氨水:Al3++4NH3•H2O═A1O2-+4NH4++2H2O | |
| D. | 在强碱溶液中次氯酸钠与Fe(0H)3反应生成Na2FeO4:3ClO+2Fe(OH)3═2FeO32-+3Cl-+H2O+4H+ |
 (6)氯仿 (7)三氯甲烷(8)臭氧(9)氧气
(6)氯仿 (7)三氯甲烷(8)臭氧(9)氧气