题目内容
10.现有9种物质,分别为(1)甲苯(2)2-甲基丁烷(3)对二甲苯(4)新戊烷(5) (6)氯仿 (7)三氯甲烷(8)臭氧(9)氧气
(6)氯仿 (7)三氯甲烷(8)臭氧(9)氧气其中属于烃的是(1)(2)(3)(4),属于芳香族化合物的是(1)(3)(5),属于同系物的是(1)(3),互为同分异构体的是(2)(4),属于同种物质的是(6)(7),属于同素异形体的是(8)(9).
分析 烃是仅含有碳氢元素的化合物;
芳香族化合物是含有苯环的有机化合物;
结构相似、分子组成相差若干个“CH2”原子团的有机化合物互相称为同系物;
具有相同分子式而结构不同的化合物互为同分异构体;
同素异形体是同种元素形成的不同单质.据此分析.
解答 解:(1)甲苯分子中只含有碳氢两种元素,属于烃,含有苯环属于芳香族化合物;
(2)2-甲基丁烷分子中只含有碳氢两种元素,属于烃;
(3)对二甲苯分子中只含有碳氢两种元素,属于烃,含有苯环属于芳香族化合物,与甲苯互为同系物;
(4)新戊烷分子中只含有碳氢两种元素,属于烃,与2-甲基丁烷具有相同分子式而结构不同,互为同分异构体;
(5) 分子中含有苯环属于芳香族化合物;
分子中含有苯环属于芳香族化合物;
(6)氯仿的分子式为CHCl3,不属于烃,其名称为三氯甲烷;
(7)三氯甲烷的分子式为CHCl3,不属于烃,与氯仿是同种物质;
(8)臭氧是O元素的一种单质;
(9)氧气是O元素的一种单质,与臭氧是同素异形体;
属于烃的是(1)(2)(3)(4);属于芳香族化合物的是(1)(3)(5),属于同系物的是(1)(3),互为同分异构体的是(2)(4);属于同种物质的是 (6)(7),属于同素异形体的是(8)(9);
故答案为:(1)(2)(3)(4);(1)(3)(5);(1)(3);(2)(4);(6)(7);(8)(9).
点评 本题考查了同系物、同分异构体、同素异形体、同位素等概念以及烃、芳香化合物的判断,难度不大,根据概念判断即可,侧重于考查学生对基础知识的应用能力.

练习册系列答案
相关题目
1.化学与社会生活紧密相关,下列说法不正确的是( )
| A. | 大量塑料废弃物会造成严重的白色污染,应将其焚烧处理 | |
| B. | 应用放射性同位素发射出的射线,可进行食物保鲜和肿瘤治疗 | |
| C. | 过度开采使用煤、石油等化石燃料,会导致空气中PM2.5浓度升高 | |
| D. | 近两年全国普遍取消了各种节日焰火晚会,对减缓空气污染起到了一定作用 |
18.25℃时,在25.00mL 0.1000mol•L-1CH3COOH中滴入0.1000mol•L-1的氢氧化钠溶液,溶液的pH与所加氢氧化钠溶液的体积关系如图所示.已知0.1000mol•L-1CH3COOH的电离度为1.33%,下列有关叙述正确的是( )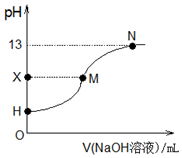

| A. | 酸碱滴定选用指示剂:甲基橙试液 | |
| B. | H点处的溶液:pH<3 | |
| C. | X=7时,M点对应加入氢氧化钠溶液的体积:25.00 mL | |
| D. | H、M、N三点各自对应的溶液:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
5.二氧化氯(ClO2)是极易溶于水且不发生化学反应的黄绿色气体,沸点为11℃,可用于处理含硫废水.某小组在实验室中探究ClO2与Na2S的反应.回答下列问题:
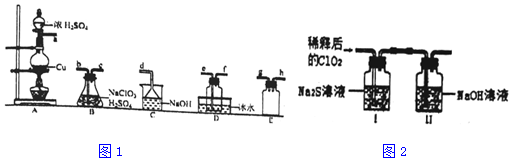
(1)ClO2的制备(已知SO2+2NaClO3+H2SO4═2ClO2↑+2NaHSO4)置A中反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O.
②欲收集干燥的ClO2,选择图1中的装置,其连接顺序为a→g→h→b→c→e→f→d(按气流方向,用小写字母表示)
③装置D的作用是冷凝并收集ClO2.
(2)ClO2与Na2S的反应
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入图2所示装置中充分反应,得到无色澄清溶液.一段时间后,通过下列实验探究I中反应的产物.
④ClO2与Na2S反应的离子方程式为8ClO2+5S2-+4H2O=8Cl-+5SO42-+8H+.

(1)ClO2的制备(已知SO2+2NaClO3+H2SO4═2ClO2↑+2NaHSO4)置A中反应的化学方程式为Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+H2O.
②欲收集干燥的ClO2,选择图1中的装置,其连接顺序为a→g→h→b→c→e→f→d(按气流方向,用小写字母表示)
③装置D的作用是冷凝并收集ClO2.
(2)ClO2与Na2S的反应
将上述收集到的ClO2用N2稀释以增强其稳定性,并将适量的稀释后的ClO2通入图2所示装置中充分反应,得到无色澄清溶液.一段时间后,通过下列实验探究I中反应的产物.
| 操作步骤 | 实验现象 | 结论 |
| 取少量I中溶液于试管甲中,滴加品红溶液和盐酸 | 品红始终不褪色 | ①无_SO2(或HSO3-或SO32-)生成 |
| 另取少量I中溶液于试管乙中,加入Ba(OH)2溶液,振荡 | ②白色沉淀 | 有SO42- |
| ③继续在试管乙中滴加Ba(OH)2溶液至过量,静置,取上层清液于试管丙中,________ | 有白色沉淀生成 | 有Cl-生成 |
15.设NA为阿伏伽德罗常数的值.下列有关叙述正确的是( )
| A. | 硝酸与铜反应得到NO2、N2O4共23g,则铜失去的电子数为0.5NA | |
| B. | 10g 46%的乙醇水溶液中所含氢原子数目为0.6NA | |
| C. | 标准状况下8.96L的平均相对分子质量为3.5的H2与D2含有中子数0.3NA | |
| D. | 1molCu与足量的S完全反应,转移电子数为2NA |
2.下列反应属于吸热反应的是( )
| A. | 钠与水反应 | B. | 甲烷在空气中燃烧 | ||
| C. | 盐酸与氢氧化钠溶液反应 | D. | 碳与二氧化碳高温反应 |
19.短周期元素a、b,c、d、e在周期表中的位置如图,下列说法正确的是( )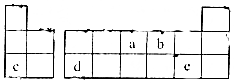

| A. | 气态氢化物的稳定性:a>b>c | |
| B. | 原子半径大小:a>b>c | |
| C. | c,d,e的氧化物对应的水化物之间两两皆能反应 | |
| D. | b、c形成的化合物中阴、阳离子的个数比为1:2 |
20.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 16 g O2和O3 的混合气体中含有的分子数为0.5 NA | |
| B. | 25℃时,Ksp(BaSO4)=1×10-10,则BaSO4饱和溶液中Ba2+数日为1×10-5 NA | |
| C. | 标准状况下,2.24 L Cl2 通入足量H2O或NaOH溶液中转移的电子数均为0.1 NA | |
| D. | 常温下,1 mol的NaHCO3固体中含HCO3-的数目为NA |